Sommario: 2.1 I parametri di esplosione – 2.2 Le miscele ibride – 2.3 Le miscele infiammabili in atmosfere arricchite d’ossigeno – 2.4 Esempi applicativi ed approfondimenti – 2.5 Parametri caratteristici di alcune sostanze
Abstract: Nel Capitolo si introducono i principali parametri di esplosione delle miscele ATEX dovute a gas, vapori, nebbie e polveri combustibili e vengono esposti alcuni esempi applicativi e approfondimenti.
«Se si strofina l’ambra con un panno avvengono piccoli fenomeni curiosi: si sente un crepitio, al buio si vedono scintille, pagliuzze e bruscoli di carta che vengano accostati danzano come impazziti. L’ambra in greco si chiama electron; fino al 1600 questi effetti non erano stati osservati su altre sostanze, e perciò sono stati chiamati effetti elettrici.»
Primo Levi1
Molte possono essere le conseguenze di un’esplosione che si origini in un luogo di lavoro ed è consuetudine differenziare gli scenari di incidente a seconda che i medesimi abbiano inizio da rilasci di gas2, vapori, nebbie3, spray4 oppure da polveri combustibili5. Tali scenari incidentali mostrano caratteristiche di esplosione molto differenti, nonostante la presenza di proprietà simili in termini di parametri di accensione e combustione (Eckhoff, 2005). Tutte le sostanze originate da un rilascio accidentale presentano, infatti:
-
campi di esplodibilità sufficientemente definiti (LEL o LFL, UEL o UFL);
-
velocità di combustione laminare;
-
relazione tra turbolenza e velocità di combustione laminare;
-
fenomeno di transizione tra deflagrazione e detonazione;
-
rapporto di incremento di pressione in caso di esplosione isocora6;
-
rapporto di incremento di volume in caso di esplosione isobara;
-
minima energia di accensione (MIE);
-
temperatura di accensione per date condizione di test.
Queste similarità hanno portato molti autori ed enti normativi a concludere che le esplosioni di gas/vapori risultino assimilabili a quelle derivanti da ATEX generate da polveri combustibili. Così non è.
A fronte delle analogie indicate sono presenti differenze sostanziali.
Una prima distinzione è legata all’intima miscelazione che avviene tra gas e vapori con l’aria comburente, in particolare in zone confinate e a ridotta ventilazione. La concentrazione dei gas e vapori con l’aria permane costante nel tempo in assenza di ventilazione7; tale fenomeno non è analogo per le polveri e per le gocce di liquidi (spray e nebbie) che palesano invece un moto controllato da forze di inerzia e gravitazionali, le quali non hanno alcuna influenza nella miscelazione di gas e vapori. La sensibilità a tali forze appare inoltre strettamente dipendente dal diametro di polveri e gocce e dalla velocità locale dell’aria.
Un’ulteriore diversità tra i comportamenti è correlata alla presenza di una certa turbolenza locale dell’aria; questo parametro, mentre nei gas e vapori non modifica le concentrazioni di regime eventualmente già raggiunte, con le polveri aumenta la durata della sospensione (e quindi la durata dell’ATEX). La medesima turbolenza, nel caso di spray, può dar luogo alla coalescenza della dispersione che necessita di ulteriori approfondimenti da parte dell’analista.
Inoltre, mentre è possibile trasportare gas e liquidi infiammabili in assenza di comburente, il convogliamento delle polveri combustibili necessita sempre di un gas vettore che generalmente è aria (molto costoso, infatti, risulterebbe l’utilizzo di gas inerti quali azoto e CO2).
Infine, lo stoccaggio: per i gas e vapori è possibile attuare tale operazione tenendo sotto controllo i parametri sensibili come la concentrazione media della sostanza in aria, strategia che con le polveri oltre ad essere difficoltosa, risulta inaffidabile. Infatti, mentre la rilevazione localizzata della concentrazione dei gas presenti in uno stoccaggio può essere sufficientemente rappresentativa della concentrazione che si registra in tutto il volume chiuso, per le polveri questa considerazione non possiede la medesima valenza.
Ad ogni modo, a prescindere dalle differenze indicate, nell’ambito dell’analisi delle esplosioni industriali è consuetudine, comunque, procedere ad una caratterizzazione delle sostanze pericolose attraverso parametri quantitativi che permettano di classificare ogni aspetto legato alla stabilità o reattività della sostanza analizzata. Nel seguito si propone una sintesi dei principali parametri utilizzati per quantificare il rischio di esplosione nelle sostanze/miscele allo stato di liquido, vapore, nebbia, spray o polvere combustibile.
2.1 I parametri di esplosione
2.1.1 I limiti di esplosione
I limiti di esplosione rappresentano i confini del campo di esplosione nel quale la concentrazione della sostanza infiammabile nell’aria può dar luogo ad un’esplosione (deflagrazione o detonazione). Esiste pertanto un limite inferiore di esplosione (LEL, Lower Explosion Limit) e un limite superiore di esplosione (UEL, Upper Explosion Limit).
Tali acronimi, nell’ambito degli standard CEI EN 60079-10-1:2016 e EN IEC 60079-10-1:2021 sono stati modificati in, rispettivamente, LFL e UFL (lower e upper flammable limits) come avremo modo di constatare nel Capitolo 4. Poiché tale modifica appare più formale che sostanziale, come verrà spiegato più avanti, nel presente manuale utilizzeremo indifferentemente le due formulazioni quali sinonimi le une delle altre8.
I limiti di esplosione sono misurati in miscela con l’aria. Tali limiti, nel caso di gas, vapori e nebbie, si modificano al variare delle condizioni al contorno nelle quali sono quantificati. In particolare:
-
l’aumento della concentrazione di ossigeno amplia notevolmente l’UEL, e quindi il campo di esplosione, mentre ha scarsa influenza sul LEL (Figura 2.1);
-
un aumento di temperatura tende ad aumentare il campo di esplosione con un incremento dell’UEL;
-
un aumento deciso del campo di esplosione si registra invece con l’aumento della pressione che determina un forte spostamento dell’UEL.
Alcune equazioni empiriche permettono di correlare i limiti di esplosione alla temperatura (Zabetakis et al., 1959; Crowl et al., 2002):


dove:
| ∆Hc | è il calore netto di combustione (kcal/mole) |
| T | è la temperatura (°C) |
Il pedice 25 indica il riferimento alla temperatura dell’ambiente
Anche la pressione influenza il campo di esplosione, con la modifica dell’UEL, secondo la seguente relazione (Zabetakis, 1965; Crowl et al., 2002):

dove:
| P | è la pressione (MPa assoluti) |
I limiti di esplosione (LEL, UEL) si esprimono generalmente in % o in g/m3. Nel caso di miscele ATEX, composte da più sostanze infiammabili, il LEL (e UEL) complessivo si calcola con l’ausilio della legge di Le Chatelier (eq. 2.4)

Dove yi è la frazione molare o volumetrica della i-esima sostanza.
Nel caso delle polveri combustibili il solo limite di esplosione comunemente rilevato è il LEL, (nell’ambito di pubblicazioni specializzate e di alcuni laboratori, il limite inferiore di esplosione per le polveri viene definito MEC, minimum explosible concentration. Nel presente lavoro si è scelto, per semplicità di trattazione, di accorpare i termini per gas e per polveri combustibili) essendo l’UEL poco utilizzato nella corrente pratica applicativa (risulta difficile realizzare il monitoraggio della concentrazione delle polveri, soprattutto all’interno dei contenimenti). In genere, l’UEL supera il LEL di almeno due ordini di grandezza essendo compreso tra 2 e 3 kg/m3.
Una così grande differenza tra LEL e UEL non si rinviene nel caso dei gas e vapori; gli idrocarburi, per esempio, possiedono un rapporto UEL/LEL che non supera, in genere, il fattore 10. Per converso esiste un ristretto numero di sostanze (gas o vapori) che sono esplosive anche in concentrazione del 100%. Discutiamo di: acetilene, monovinilacetilene, propil nitrato, isopropil nitrato, ossido di etilene e idrazina.
Anche il LEL nelle polveri varia al variare delle condizioni ambientali e di condizione granulometrica. I principali motivi di modifica sono i seguenti:
-
un aumento della percentuale di ossigeno tende a far diminuire il LEL delle polveri combustibili;
-
il LEL diminuisce al diminuire del diametro medio delle polveri combustibili.
Il LEL nelle polveri combustibili è espresso in g/m3 e risulta frequentemente compreso tra 15 e 30 g/m3.
Nel caso di spray e nebbie i parametri LEL e UEL non risultano, invece, adeguati alla comprensione e classificazione del fenomeno legato alla formazione di ATEX. In ogni caso gli spray (d > 100 µm) e le nebbie (d < 100 µm) con concentrazioni in massa superiori a 40 g/m3 sono da ritenersi esplosive (Hattwig et al., 2004)9.
La presenza di nebbie e spray influenza, però, i limiti di infiammabilità già indicati per i gas e vapori, come di seguito illustrato. Per sospensioni con diametri medi di goccia inferiori a 0,01 mm, il LEL risulta sostanzialmente analogo a quello della medesima sostanza in forma di vapore. Questo fenomeno risulta altresì presente anche alle basse temperature, in assenza di vapori della sostanza infiammabile. Nebbie di questa tipologia di dimensione si formano molto spesso durante le fasi di condensazione (es. interno di reattori di processo in fase di raffreddamento).
Invece, per spray generati meccanicamente, aventi diametro medio di goccia compreso tra 0,01 mm e 0,2 mm, il LEL diminuisce con l’aumentare del diametro della goccia. Dati sperimentali evidenziano come, in corrispondenza dei diametri medi di goccia più elevati, il LEL dello spray risulta pari a meno di un decimo del LEL del vapore corrispondente. Infine, quando gli spray raggiungono diametri medi di goccia compresi tra 0,6 mm e 1,5 mm, la propagazione della fiamma risulta inibita.
La Normativa di riferimento per l’esecuzione dei test è la seguente: UNI EN 1839 (LEL e UEL per gas e vapori), UNI EN 14034-3 (LEL per polveri combustibili).
Il LEL (per gas/vapori) risulta generalmente utilizzato per il dimensionamento dei sistemi di controllo di esplosione mentre l’UEL (per gas/vapori) risulta utile nel caso si voglia evitare il campo di esplosione utilizzando la strategia di saturazione dei vapori in serbatoi di stoccaggio di infiammabili. Il LEL delle polveri può essere utile a determinare la presenza o meno dell’ATEX in flussi pneumatici di trasporto.
Figura 2.1 – Diagramma di infiammabilità in condizioni di temperatura e pressione ambiente
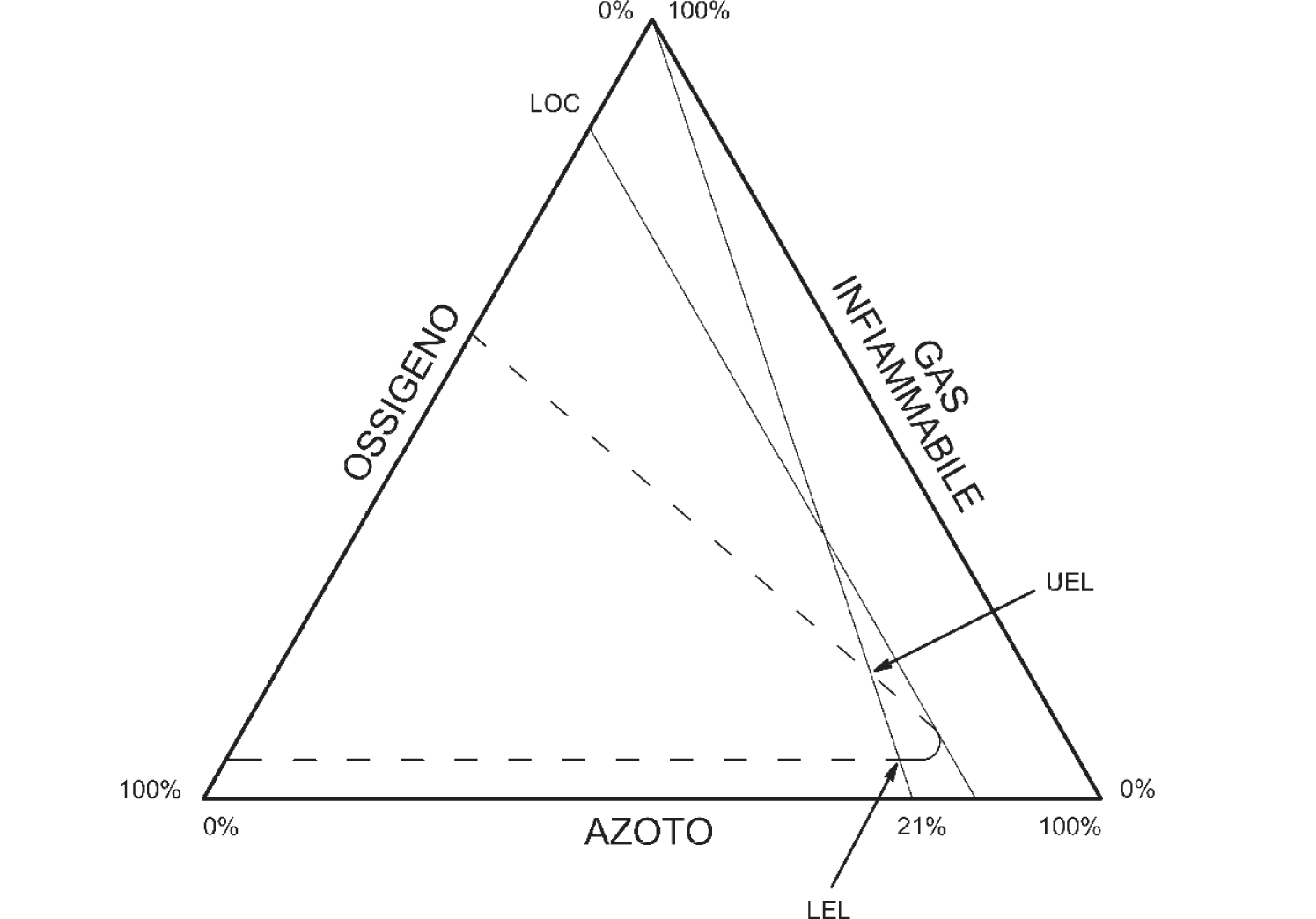
Fonte: Crowl et al., 2002
2.1.2 Concentrazione limite di ossigeno (LOC)
La concentrazione limite di ossigeno (Limiting Oxygen Concentration, LOC) è la massima concentrazione di ossigeno (determinata in condizioni di prova specificate) in una miscela di sostanza infiammabile, aria e un gas inerte in corrispondenza della quale non si verifica un’esplosione.
Al di sotto del LOC la miscela non è in grado di generare una reazione che si autosostenga e si propaghi all’insieme della miscela incombusta. Come infatti si rileva in Figura 2.1, al di sotto della concentrazione limite di ossigeno, il campo di esplosione si chiude completamente.
Il LOC dipenderà sia dal tipo di sostanza testata sia dal gas utilizzato per la generazione dell’atmosfera inerte.
Le norme tecniche di riferimento per l’esecuzione dei test sono la ASTM E2079 per i gas e vapori e la EN 14034-4 per le polveri combustibili.
La determinazione di questo parametro è posta a fondamento delle operazioni di prevenzione dell’ATEX definite inertizzazione. Tale tecnica, come vedremo in seguito, si suddivide in inertizzazione per flussaggio e inertizzazione per purgaggio (in pressione o sottovuoto).
Nel caso degli idrocarburi è possibile una determinazione approssimata del LOC attraverso una procedura di calcolo semplificata che richiede la conoscenza del LEL e della stechiometria di reazione (Crowl et al., 2002).
2.1.3 Temperatura di accensione
La temperatura di accensione rappresenta, convenzionalmente, la minima temperatura di una superficie riscaldata in corrispondenza della quale, in condizioni specificate, avviene l’accensione di un’ATEX.
I gas e vapori presentano un’unica temperatura di accensione (Ti, Autoignition Temperature oppure Tacc secondo la notazione presente nella ex Guida CEI 31-35:2012 (ora abrogata) mentre le polveri combustibili possiedono due tipi di temperature di accensione: la temperatura di accensione della nube di polvere (Tcl, Cloud Temperature) e la temperatura di accensione dello strato di polvere (Tlayer oppure T5mm nel caso di presenza di uno strato standard di polvere dello spessore pari a 5 mm).
Si sottolinea che tale parametro non rappresenta un aspetto univocamente definibile e sperimentalmente rilevabile. Esso infatti risulta marcatamene dipendente dalle modalità di esecuzione del test. In generale, la temperatura di accensione tende a diminuire al crescere della superficie calda esposta all’ATEX e al diminuire della velocità con la quale l’ATEX lambisce la medesima superficie calda. Inoltre esistono sostanze che manifestano comportamenti anomali rispetto a questo parametro10.
La Normativa a cui fare riferimento per l’esecuzione dei test è la UNI EN 14522 (per gas/vapori) e CEI EN 50281-2-1 (per le polveri combustibili).
Per gli apparecchi elettrici, soggetti ad ATEX gas, è prevista una notazione standard che indica la massima temperatura raggiungibile dagli stessi (Tabella 2.1).
Tabella 2.1 – Limite di temperatura superficiale e classe di temperatura dell’apparecchio elettrico
| Classe di temperatura | Limite di temperatura (°C) |
|---|---|
| T1 | 450 |
| T2 | 300 |
| T3 | 200 |
| T4 | 135 |
| T5 | 100 |
| T6 | 85 |
La temperatura di accensione è normalmente testata grazie al riscaldamento di superfici pulite.
La temperatura di accensione rappresenta un parametro indispensabile per l’individuazione delle massime temperature superficiali degli apparecchi (elettrici e non elettrici) collocati e destinati a funzionare in atmosfera potenzialmente esplosiva.
2.1.4 Minima energia di accensione
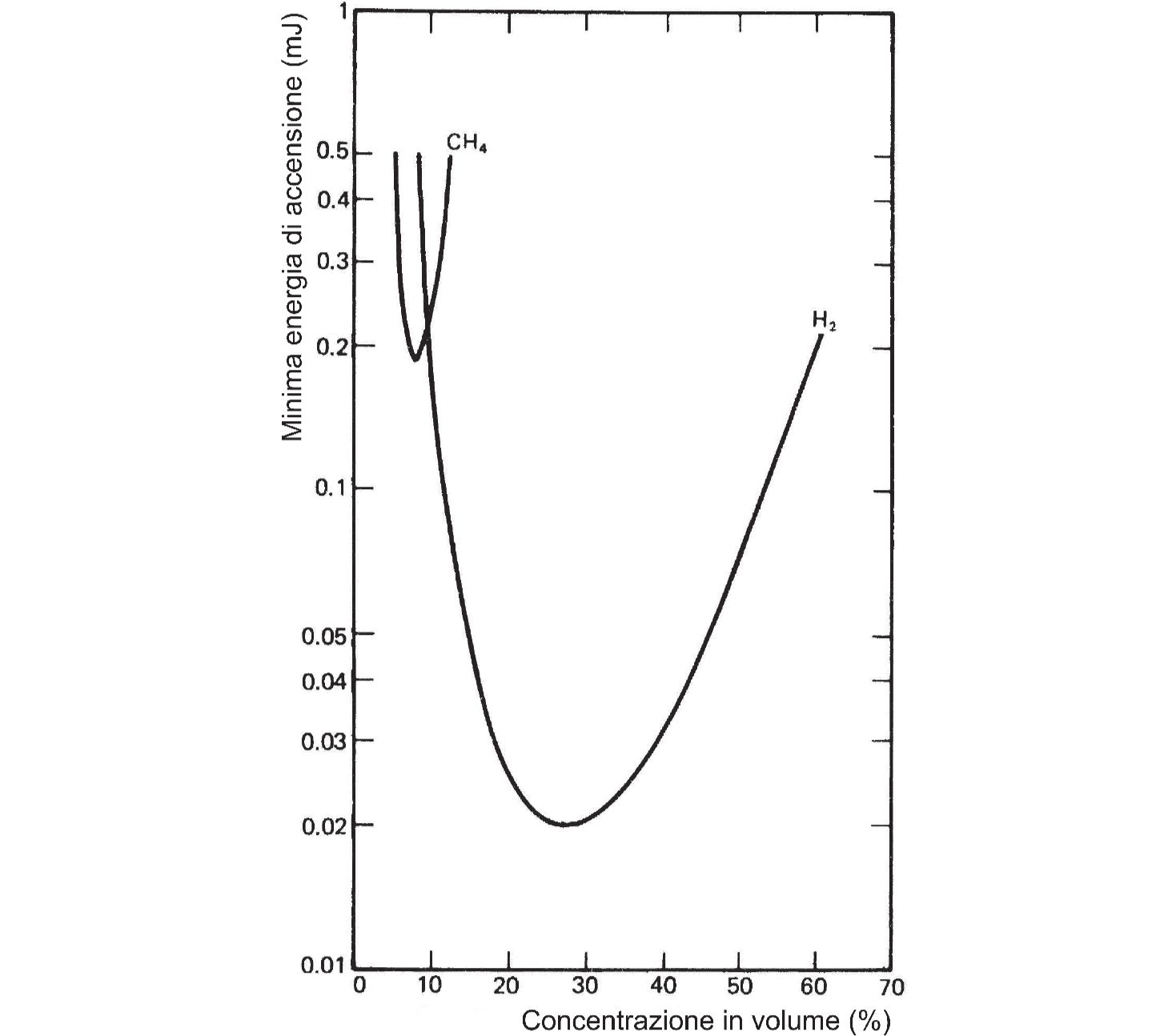
La minima energia di accensione (MIE, Minimum Ignition Energy) è l’energia che, in condizioni di prova specificate, risulta in grado di innescare l’ATEX sottoposta a test. Essa rappresenta sia per i gas e vapori (Figura 2.2) sia per le polveri combustibili, un indice di sensibilità all’innesco, utile al dimensionamento degli apparecchi a sicurezza intrinseca e alla valutazione del rischio di innesco elettrostatico.
L’energia minima di innesco, nel caso delle costruzioni elettriche collocate in ATEX dovute a gas e vapori, viene suddivisa nelle categorie IIA, IIB, IIC, con modo di protezione “d” (= a prova di esplosione), in funzione dell’interstizio sperimentale massimo di un giunto standard che non permetta ad un’eventuale esplosione avvenuta all’interno di una custodia di propagarsi all’esterno (MESG). Si ha, quindi:
-
Gruppo IIA: MESG > 0,9 mm
-
Gruppo IIB: 0,5 mm ≤ MESG ≤ 0,9 mm
-
Gruppo IIC: MESG < 0,5 mm
Il modo di protezione “i” (= sicurezza intrinseca), prevede invece che la suddivisione IIA, IIB, IIC sia fondata sul parametro definito corrente minima di accensione (MIC).
Figura 2.2 – Relazione tra MIE e concentrazione per metano e idrogeno
A fini prevenzionistici e di valutazione del rischio può essere utile la conversione dei valori del MESG in MIE attraverso la seguente Figura 2.3.
Figura 2.3 – Relazione tra MESG e MIE
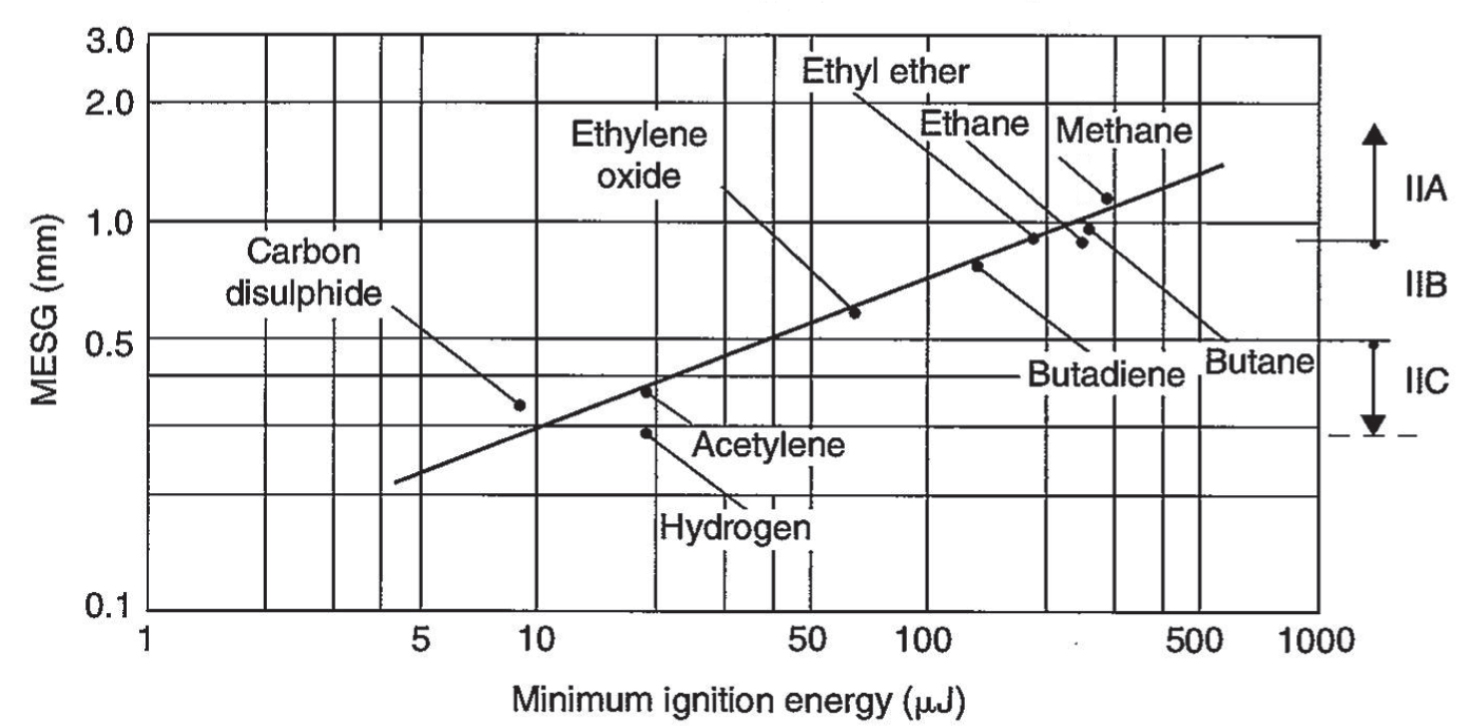
Fonte: Groh, 2004
La retta di interpolazione logaritmica tra MIE e MESG possiede la seguente equazione approssimata:
dove il MESG è espresso in mm e la MIE è espressa in µJ.
I gruppi di gas potranno dunque essere classificati, in prima approssimazione, secondo quanto riportato in Tabella 2.2, nella quale si evidenza il legame con la MIE (mediato dal MESG).
Tabella 2.2 – Relazione tra gruppo di gas e MIE
| Gruppo di Gas | MIE interpolata con l’equazione 2.5 | MIE tipica (IEC 60079-0) |
|---|---|---|
| IIA | MIE > 0,18 mJ | 0,2 mJ |
| IIB | 0,04 mJ ≤ MIE ≤ 0,18 mJ | 0,06 mJ |
| IIC | MIE < 0,04 mJ | 0,02 mJ |
Le costruzioni elettriche a sicurezza intrinseca collocate in ATEX derivanti da polveri combustibili saranno definibili tali se l’energia massima rilasciata dal circuito è compatibile con la classe IIB precedentemente indicata.
La minima energia di accensione, nel caso di vapori e nebbie, risulta dipendente dalle condizioni di temperatura e pressione a cui la miscela è soggetta. In generale la MIE risulta inversamente proporzionale alla pressione. All’aumento della pressione la MIE diminuisce in genere, in proporzione al quadrato della pressione, e viceversa (Hattwig et al., 2004). Analogamente la MIE si comporta all’incremento della temperatura (Moorehouse, 1974). L’espressione, approssimata, per definire tale fenomeno è la seguente:

dove:
| C | è la costante specifica; |
| P | è la pressione a cui è sottoposta la sostanza; |
| T | è la temperatura a cui è sottoposta la sostanza. |
A titolo esemplificativo si riportano in Tabella 2.3 i valori sperimentali relativi alla variazione della MIE con la diminuzione della pressione secondo quanto indicato negli studi di Pratt (1997). Risulta evidente l’incremento della MIE al diminuire della pressione assoluta.
Tabella 2.3 – Relazione sperimentale tra MIE e pressione
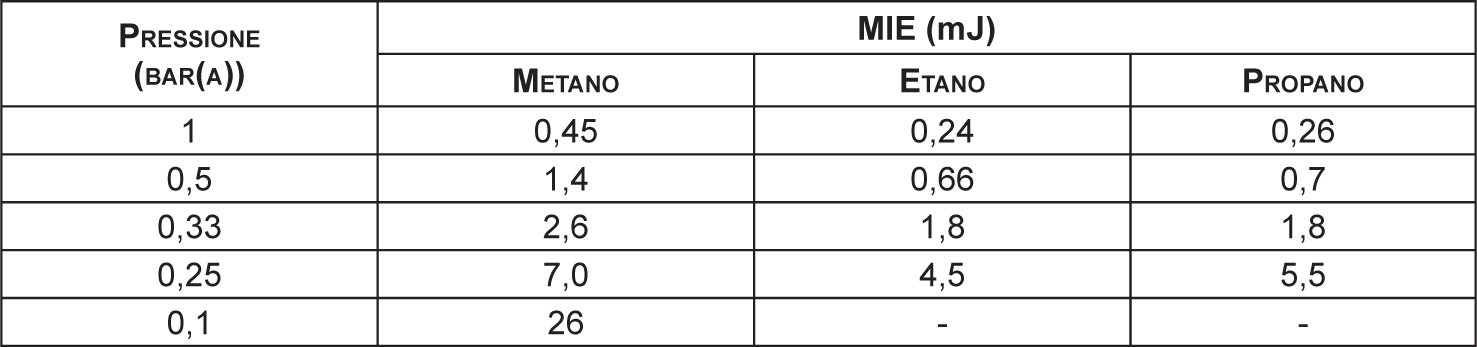
Fonte: Pratt, 1997
Nel caso delle nebbie, la MIE risulta proporzionale al d3 della dispersione. Per esempio, nel caso di nebulizzazioni di gasolio, la MIE sarà pari 10 mJ e 100 mJ rispettivamente per valori di 60 µm e 150 µm.
Le prove per la verifica sperimentale della MIE possono essere sviluppate secondo ASTM E582 per gas e vapori e UNI EN 13821 per polveri.
La MIE, nel caso delle polveri combustibili, risulta correlata alla granulometria; a parità di composizione le frazioni fini tendono a possedere energie di innesco più basse rispetto a polveri grossolane.
La MIE, inoltre, tende a decrescere con:
-
l’aumento della temperatura della miscela;
-
l’aumento della percentuale di ossigeno;
-
la diminuzione dell’umidità nella polvere.
Alcuni esempi di tali correlazione sono riportati in Figura 2.4. In genere il test di laboratorio è realizzato in apparecchi detti a tubo Hartmann oppure di tipo Mike3. I gas e vapori possiedono nella quasi totalità dei casi, MIE molto inferiori alle polveri; la MIE dei gas e vapori risulta infatti compresa tra 0,1 mJ e 0,3 mJ mentre nelle polveri oscilla (in funzione del materiale e della granulometria) tra 1 mJ e 10 J (valori inferiori a 3 mJ si manifestano soprattutto nei casi di farine molto sottili e di prodotti farmaceutici dopo operazioni di affinazione quali, per esempio, la micronizzazione).
I test di prova volti a valutare la MIE, in particolare nel caso delle polveri combustibili, sono realizzati attraverso due modalità sperimentali differenti: con o senza induttanza nel circuito di prova. La presenza dell’induttanza permette di diluire maggiormente la durata della scarica di plasma. Con questa modalità di test l’accensione risulta maggiormente efficace, rispetto alla scintilla puramente capacitiva (che invece si manifesta con modalità pressoché istantanee) e, in genere, le MIE ottenute sono minori (circa 10 volte) rispetto alle MIE capacitive.
Figura 2.4 – MIE in funzione di valor medio granulometrico e umidità della polvere (ASTM E2019)
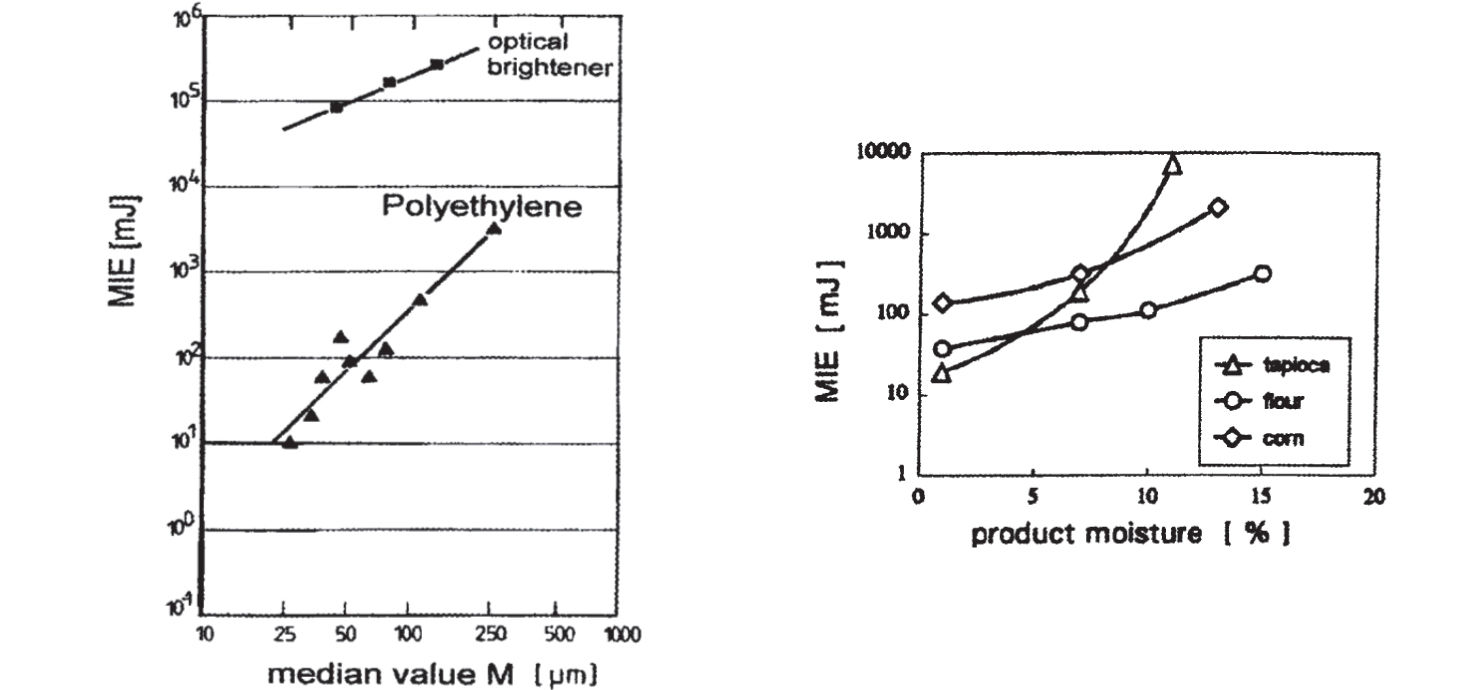
Come vedremo nel Capitolo 6, il problema che sorge è quindi quello di individuare quale valore di MIE utilizzare per le valutazioni di innesco efficace elettrostatico.
In questo senso, dato che le scariche elettrostatiche che avvengono in un impianto risultano quasi tutte di tipo capacitivo, la valutazione dei pericoli di innesco dovrebbe essere sviluppata in base ai dati di MIE ottenuti senza l’utilizzo di induttanza nel circuito (ASTM E2019).
Così come per i gas, anche la MIE delle polveri risulta particolarmente influenzata dalle condizioni di pressione e temperatura (Britton, 1999; Babrauskas, 2003). In particolare l’aumento di temperatura diminuisce la MIE linearmente (in scala logaritmica). La maggior parte delle polveri converge ad una MIE di 0,088 mJ in corrispondenza di temperature pari a 1000 °C.
L’equazione che consente la determinazione quantitativa della MIE ad una data temperatura (MIET) è la seguente:

Dove la MIE20 rappresenta la Minima Energia di Accensione della polvere misurata a 20 °C.
In generale nelle polveri l’effetto di un aumento testato di pressione fino a 1,6 bar non produce diminuzioni significative della MIE rispetto al valore atmosferico mentre una depressione testata a 0,65 bar (assoluti) manifesta un incremento che può arrivare a due volte il valore della MIE atmosferica.
Per quanto attiene, invece, la classificazione della sensibilità all’innesco elettrostatico nelle polveri combustibili, si ritiene sufficientemente conservativo lo schema riportato in Tabella 2.4 (Perry, 2005).
Da rilevare che maggior parte degli incidenti avvenuti nel passato ha avuto luogo in presenza di polveri con MIE inferiore a 25 mJ (BS 5958). In generale, tuttavia, non sono attesi inneschi di tipo elettrostatico nei casi di polveri combustibili con MIE superiori ad 1 J (NFPA, 2003).
Tabella 2.4 – MIE delle polveri combustibili e sensibilità all’accensione
| Entità della Minima Energia di Accensione delle polveri | Sensibilità all’accensione |
|---|---|
| MIE ≥ 10 mJ | Normale sensibilità di accensione |
| 3 mJ ≤ MIE < 10 mJ | Sensibilità all’accensione aumentata |
| MIE < 3 mJ | Estrema sensibilità all’accensione |
I dati riportati nel presente capitolo si riferiscono a miscele ATEX non ibride; nel caso di miscele ibride11, specifiche valutazione dovranno essere realizzate. Operativamente, quindi, la MIE oltre ad essere necessaria per la scelta degli apparecchi elettrici (gruppo di gas) collocati in ATEX, risulta indispensabile per la corretta valutazione del rischio di innesco dovuto a cariche elettrostatiche e radiofrequenze.
2.1.5 Punto di infiammabilità (Flash Point) e temperature limite di infiammabilità
Il punto di infiammabilità (FP, Flash Point) rappresenta uno tra i parametri più utilizzati per la classificazione dei liquidi infiammabili. Il FP è dunque la temperatura minima alla quale, in condizioni di prova specificate, un liquido rilascia una quantità sufficiente di gas o vapore combustibile in grado di accendersi momentaneamente all’applicazione di una sorgente di accensione efficace. Esistono molti tipi di apparecchi utilizzati per la determinazione del FP. Il liquido viene riscaldato lentamente e periodicamente è applicata una debole fiamma nella zona dei vapori; il FP è la temperatura in corrispondenza della quale si genera un flash nella zona dei vapori innescati.
In generale, il FP corrisponde, in prima approssimazione, alla Temperatura Limite Inferiore (TLI) definita da Medard12 come la temperatura alla quale il liquido vaporizzerà, in regime di saturazione, con una concentrazione di vapore corrispondente al LEL (Figura 2.5).
Figura 2.5 – Relazione tra varie proprietà di infiammabilità
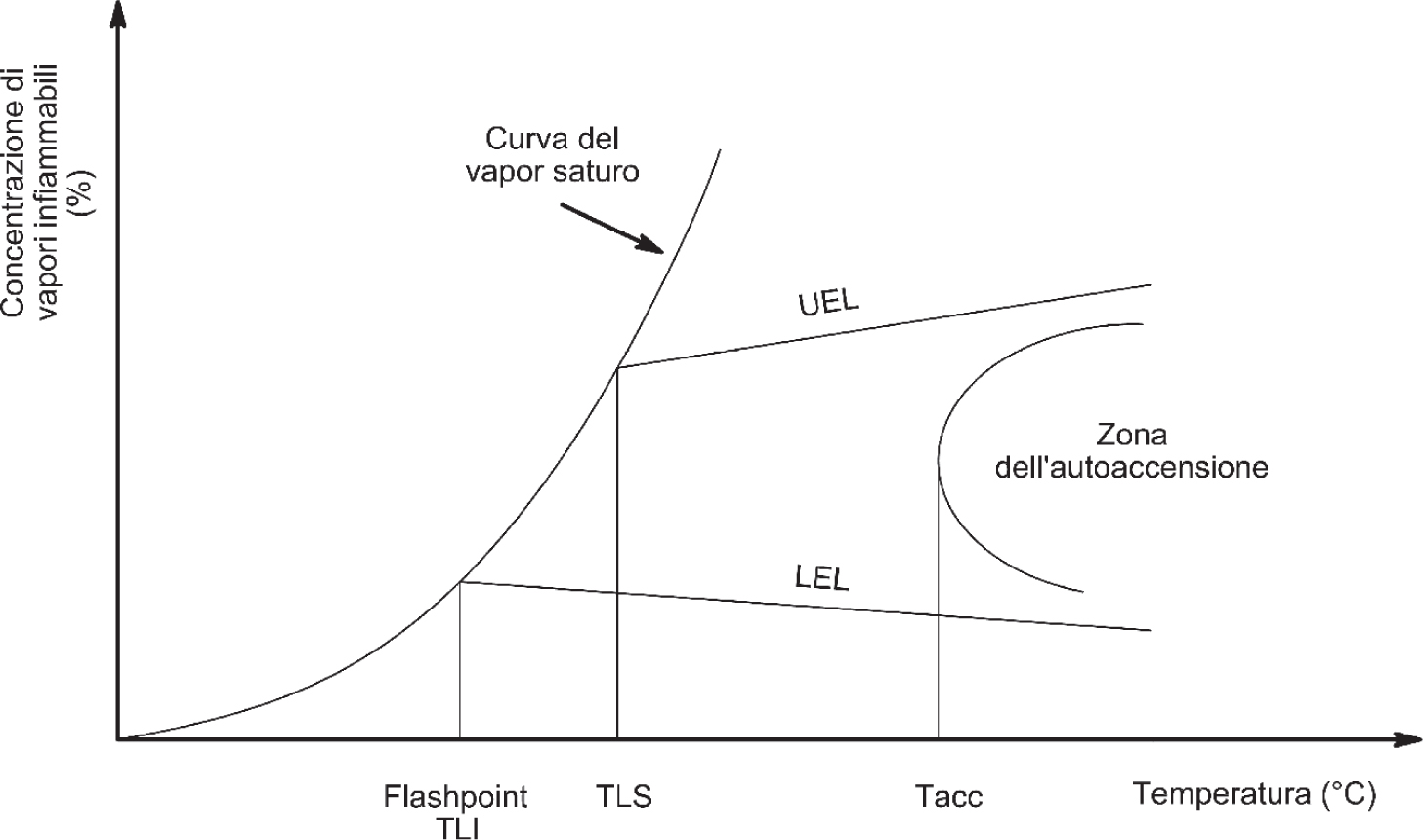
Il FP può essere inoltre correlato alla temperatura di ebollizione del liquido attraverso l’equazione seguente13:

dove:
| FP | è la temperatura di Flash Point (K); |
| a, b, c | sono costanti (Tabella 2.5) |
| Tb | è la temperatura di ebollizione del liquido (K). |
Tabella 2.5 – Constanti utilizzabili per il calcolo della temperatura di Flash Point
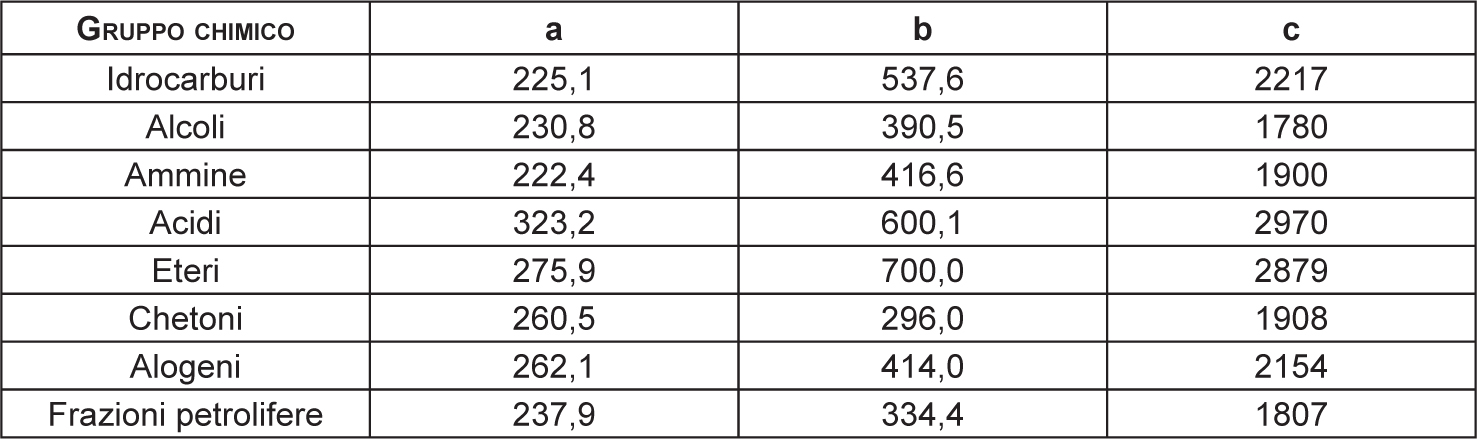
Nel caso di miscele di infiammabili, pur con le avvertenze che saranno in seguito riportate in relazione alle miscele azeotropiche, si può stimare la variazione del FP valutando il punto di ebollizione. Diminuzioni del punto di ebollizione faranno diminuire della stessa quantità il FP, per oscillazioni massime comunque entro i 10 °C.
Un altro parametro importante che consente una valutazione approfondita del livello di prevenzione dell’ATEX all’interno dei serbatoi di stoccaggio con il metodo della saturazione dei vapori, è rappresentato dalla Temperatura Limite Superiore (TLS)14 che rappresenta la temperatura in corrispondenza della quale i vapori raggiungono una concentrazione pari all’UEL (Figura 2.5).
Nel caso di serbatoi di stoccaggio di infiammabili non atmosferici, la condizione interna di prevenzione dell’ATEX è ottenibile, quindi, solo nel caso in cui la temperatura di stoccaggio risulti sufficientemente superiore alla TLS o inferiore al TLI; in queste ipotesi, infatti, la concentrazione dei vapori risulta esterna al campo di esplosione LELUEL e i vapori presenti risultano non innescabili (Medard, 1999; Ortolani, 1997).
Anche grandi escursioni delle temperature ambientali possono causare un aggravio del rischio: per esempio miscele sature al di sopra dell’UEL stoccate in serbatoi, inerti in condizioni atmosferiche, possono generare ATEX interne al campo di esplosione nel caso di una marcata diminuzione della temperatura ambientale (es. serbatoi di stoccaggio collocati in montagna, serbatoi di kerosene negli aeromobili).
Sia la TLI sia la TLS delle sostanze pure sono determinabili attraverso la tensione di vapore e i LEL e UEL, grazie all’ausilio delle seguenti equazioni:


dove:
| TLI e TLS | sono le Temperature Limite Inferiore e Superiore espresse in °C; |
| A, B e C | sono i coefficienti dell’equazione della tensione di vapore saturo di Antoine (cfr. Allegato B); |
| P0 | è la pressione ambiente (mm di Hg). |
In Tabella 2.6 sono riportati il punto di infiammabilità e la TLS per alcune sostanze. In generale si rileva una differenza tra il TLI ed il FP. Quest’ultimo parametro, misurato in coppa chiusa, risulta infatti sempre leggermente superiore al TLI di qualche grado.
Tabella 2.6 – Punto di infiammabilità e Temperatura Limite Superiore
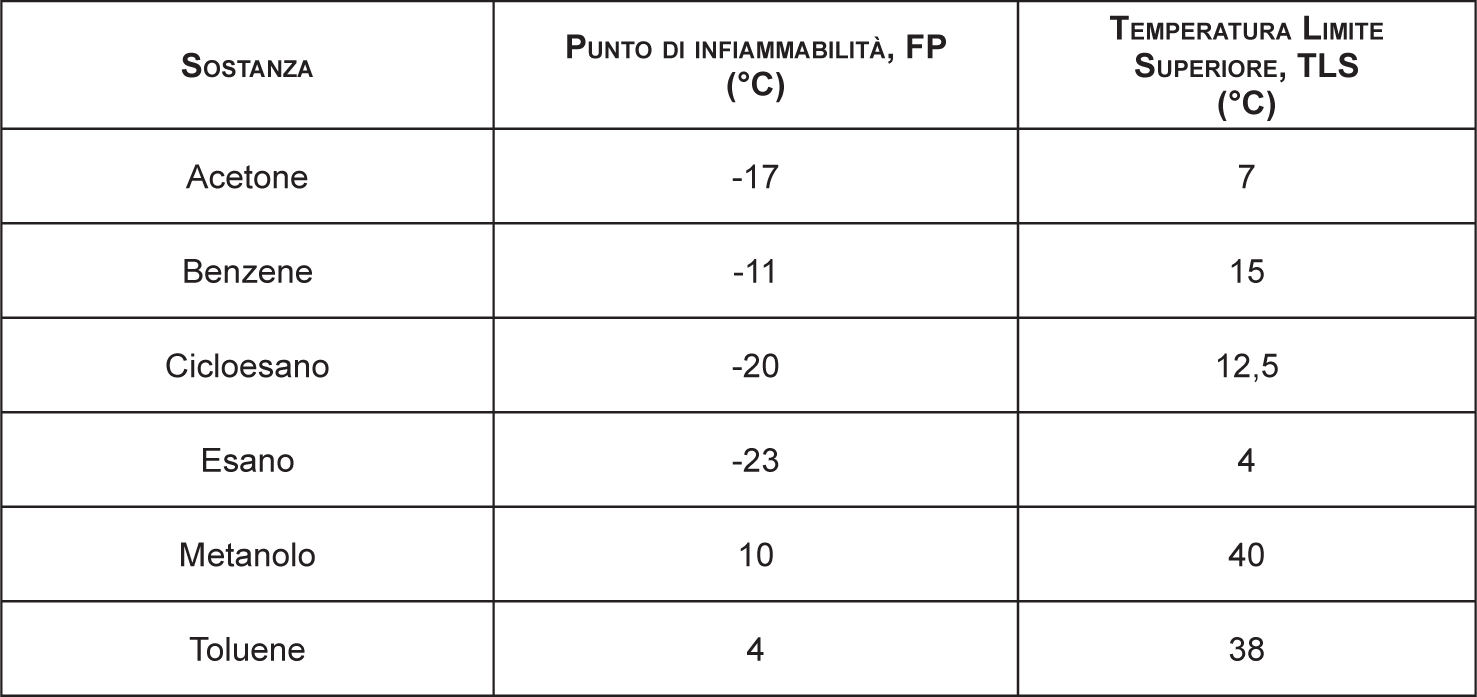
Fonte: Bretherick’s Handbook, 1999; Medard, 1999
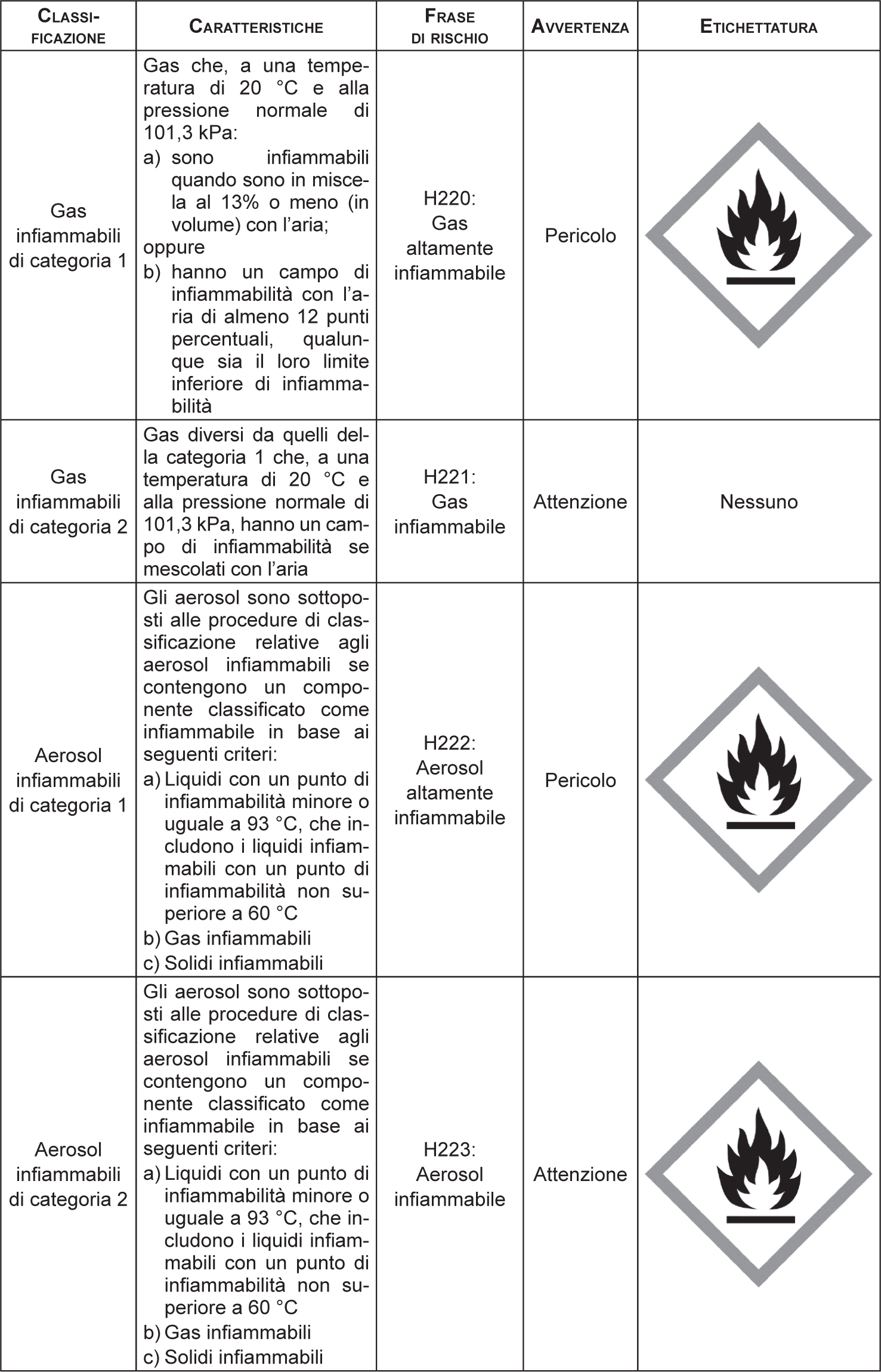
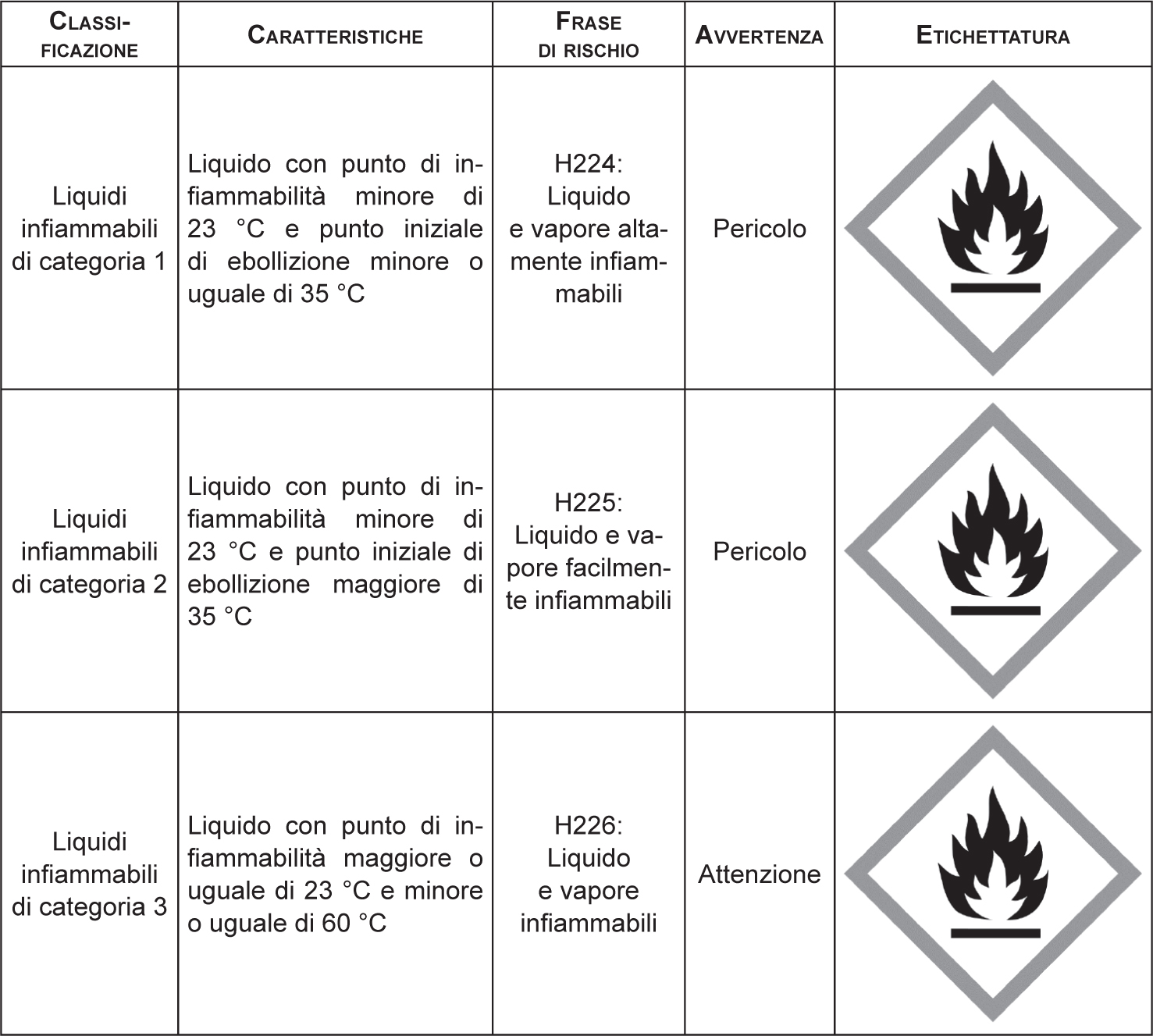
Il punto di infiammabilità rappresenta storicamente il principale parametro utile a discriminare l’attitudine all’infiammabilità dei liquidi (Tabella 2.7). A partire dal punto di infiammabilità, la Normativa infatti prevede sia nell’etichettatura sia nelle schede di sicurezza si specifichi il rischio di infiammabilità delle sostanze/miscele.
Particolare attenzione deve essere posta ai parametri di pressione e temperatura che caratterizzano la presenza della sostanza e/o miscela nel ciclo di produzione. Non sempre, infatti, la classificazione indicata in Tabella 2.7 rappresenta un riferimento assoluto per il rischio dovuto ad ATEX. Risulta infatti possibile che i parametri di processo citati possano rendere localmente non infiammabile una sostanza caratterizzata da una particolare frase di rischio (per esempio H224), questo perché l’impiego della stessa può avvenire a temperature inferiori al relativo Flash Point. Oppure, all’inverso, è possibile che liquidi non classificati secondo i dettami stabiliti in Tabella 2.7 possano generare ATEX; il caso dell’olio diatermico è, in questo senso, paradigmatico. Esso, pur non avendo particolari caratteristiche di infiammabilità (è infatti un olio combustibile), può generare ATEX-Spray fortemente micronizzate e facilmente incendiabili. Molti liquidi, infatti, anche con elevato punto di infiammabilità, quando finemente dispersi, manifestano le medesime caratteristiche di accensione dei loro vapori (Hattwig et al., 2004). Nel caso di spray e nebbie il parametro di Flash Point, quindi, non risulta adeguato alla comprensione e classificazione del fenomeno legato alla formazione di ATEX.
Tabella 2.7 – Caratteristiche di classificazione dell’infiammabilità delle sostanze e della miscele ai fini ATEX secondo il regolamento CE/1272/2008
Una interessante classificazione di liquidi e gas a fini ATEX è quella realizzata nell’ambito della Norma britannica IP15 che riportiamo in Tabella 2.8.
Tabella 2.8 – Categorie di fluido secondo IP 15
| Categoria di fluido | Descrizione |
|---|---|
| A | Liquido infiammabile che, se rilasciato, evapora rapidamente e sostanzialmente. Questa
categoria include:
|
| B | Liquido infiammabile, non di categoria A, che si trova, in occasione del rilascio, ad una temperatura superiore al suo punto di ebollizione |
| C | Liquido infiammabile, non di categoria A o B, che si trova, in occasione del rilascio, ad una temperatura superiore al suo Flash Point oppure che può venire rilasciato in forma di nebbia o spray |
| G(i) | Gas Naturale |
| G(ii) | Idrogeno di raffineria |
Operativamente l’inclusione o meno nelle precedenti categorie indicate dall’IP 15 è realizzata in funzione dei seguenti parametri (Tabella 2.9):
-
Punto di infiammabilità (Flash Point, FP);
-
Punto di ebollizione (Boiling Point, BP);
-
Condizioni di stoccaggio.
Tabella 2.9 – Relazione tra i parametri del fluido le condizioni di stoccaggio e la categoria del fluido secondo IP 15
| Classe | Descrizione | Stoccaggio sopra il FP | Stoccaggio sopra il BP | Può essere rilasciato come nebbia | Stoccaggio sotto il BP e non rilasciato come nebbia |
|---|---|---|---|---|---|
| 0 | Gas di Petrolio Liquefatto | SI | A | A | A |
| I | Flash Point inferiore a 21 °C | SI | B | C | C |
| II(1) | Flash Point compreso nell’intervallo 21-55 °C | NO | NA | C | NA |
| II(2) | Flash Point compreso nell’intervallo 21-55 °C | SI | B | C | C |
| III(1) | Flash Point compreso nell’intervallo 55-100 °C | NO | NA | C | NA |
| III(2) | Flash Point compreso nell’intervallo 55-100 °C | SI | B | C | C |
| NC(1) | Flash Point superiore a 100 °C | NO | NA | C | NA |
| NC(2) | Flash Point superiore a 100 °C | SI | B | C | C |
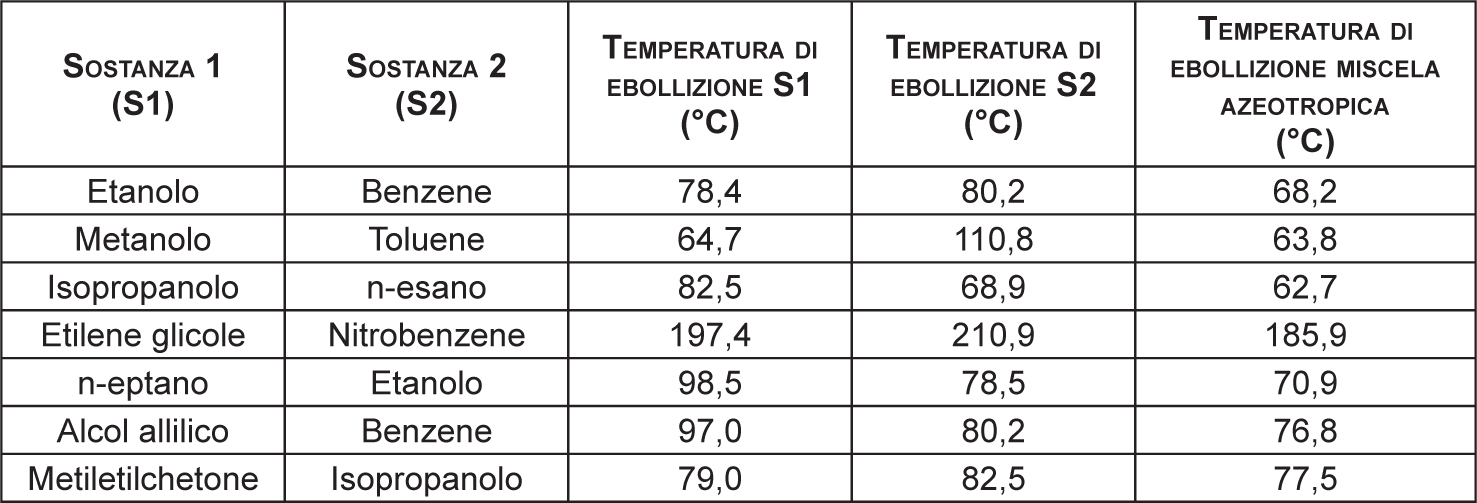
Relativamente alla classificazione prevista dall’IP15 maggiori dettagli sono riportati in Allegato G al quale si rimanda. Il caso delle miscele rappresenta un’ulteriore criticità nella valutazione dello scenario di emissione ATEX. Nell’ipotesi di miscele binarie, per esempio, il Flash Point non necessariamente risulta compreso tra i punti di infiammabilità dei singoli componenti. Nel caso di formazione di miscele azeotropiche infatti (Tabella 2.10), la tensione di vapore del preparato può risultare maggiore di quella dei singoli componenti, ed il punto di infiammabilità quindi più basso (Cardillo et al., 2008).
Un altro aspetto da valutare è relativo al livello di contaminazione degli infiammabili utilizzati nel ciclo di produzione; la presenza di componenti basso bollenti può infatti causare una radicale modificazione delle caratteristiche di infiammabilità del preparato, aggravando il rischio di incendio/esplosione.
Tabella 2.10 – Alcuni esempi di temperature di ebollizione di miscele azeotropiche
Anche l’aggiunta di acqua ad una sostanza infiammabile (e miscibile), può determinare la creazione di miscele azeotropiche con un Flash Point sensibilmente più basso dell’infiammabile di partenza. Tuttavia le sostanze non azeotropiche con l’acqua (es. metanolo), beneficiano sempre dell’introduzione in miscela della stessa al fine di ridurre l’infiammabilità complessiva del preparato, come vedremo nella parte che tratterà la prevenzione della formazione di ATEX (Figura 2.6).
Figura 2.6 – Dipendenza del punto di infiammabilità nelle miscele di differenti alcol con acqua
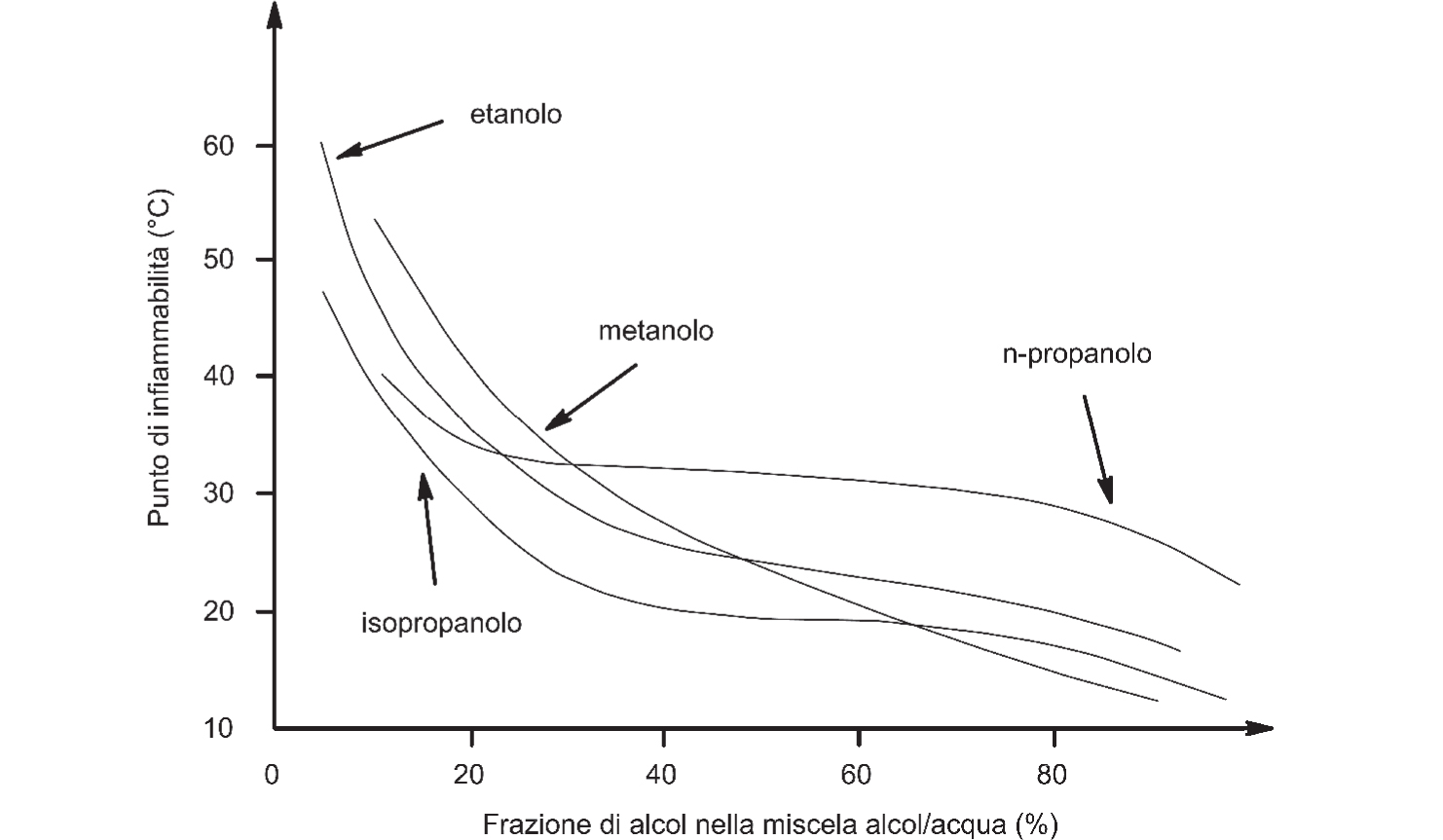
Fonte: Hattwig et al., 2004
Le principali Normative per la determinazione del punto di infiammabilità sono la UNI EN 22592 (test in vaso aperto) e UNI EN 22719 (test in vaso chiuso). A parità di sostanza analizzata, il test in vaso chiuso è più conservativo e normalmente restituisce valori di temperatura inferiori rispetto a quelli ottenuti in vaso aperto. Questo probabilmente a causa di movimenti d’aria che, con il metodo a vaso aperto, contribuiscono a diluire parzialmente le concentrazioni di vapore nella zona di accensione. Non esistono invece standard internazionali riconosciuti per la determinazione delle temperature limite superiore ed inferiore.
2.1.6 Velocità di combustione
Un ulteriore parametro utile a caratterizzare il rischio dovuto ad esplosioni è la velocità di combustione laminare e la velocità del fronte di fiamma. La velocità di combustione laminare (Su) rappresenta la velocità di propagazione del fiamma misurata al netto dell’effetto di espansione dei gas combusti mentre la velocità del fronte di fiamma (Sf) contempla l’effetto di espansione di tali gas secondo la relazione seguente (Genova et al., 2001):
dove E parametrizza l’espansione dei gas combusti.
Naturalmente, alla stregua di buona parte dei parametri di esplosione, la velocità di combustione laminare varia al variare delle condizioni al contorno (pressione, temperatura, concentrazione dell’infiammabile). Quanto più sarà rilevante il rilascio di ATEX da cui ha origine la fiamma, tanto più il fronte di fiamma accelererà a causa dell’espansione termica dei gas combusti. Alcuni esempi di velocità di combustione laminare per gas e vapori sono i seguenti (NFPA 68): acetone (Su= 0,54m/s), metano: (Su= 0,40m/s), idrogeno: (Su = 3,12m/s).
La velocità di combustione laminare delle polveri combustibili oscilla invece nel range compreso tra 0,05m/s e 0,65m/s (Nagy et al., 1983; Eckhoff, 2003), in funzione della tipologia di test realizzato.
2.1.7 Granulometria delle polveri
La granulometria delle polveri è un parametro valutato e tipicamente utilizzato per includere (o escludere) le polveri combustibili nel campo di applicazione del Titolo XI, D.Lgs. n. 81/2008. In generale, le polveri combustibili con frazioni granulometriche inferiori a 500µm si devono ritenere capaci di generare ATEX15. Risulta quindi evidente che, ove il test si esegua con lo scopo di dedurne importanti conseguenze in termini di prevenzione e protezione contro il rischio di esplosione (es. escludere il rischio dovuto alla presenza di ATEX nella parte di impianto/lavorazione oggetto di analisi), sarà necessaria una pianificazione nei prelievi sul ciclo di produzione delle polveri che consenta di ottenere un campione realmente rappresentativo delle polveri presenti nell’impianto o nel sistema da analizzare.
È quindi consigliabile la valutazione dell’affidabilità del campionamento stesso, attraverso una verifica con la distribuzione statistica t-Student, adatta ai piccoli campionamenti (cfr. Allegato C).
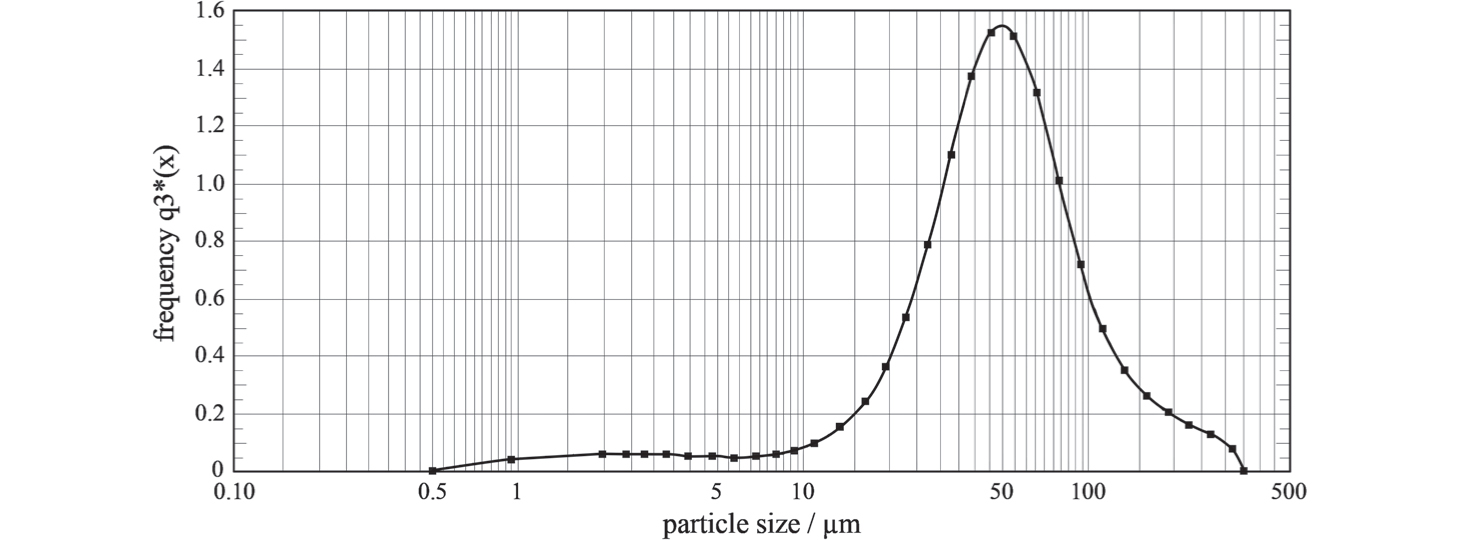
In Figura 2.7 è rappresentata la distribuzione granulometrica di una polvere combustibile che evidentemente che può generare ATEX.
Un’ulteriore possibilità di approfondimento che viene permessa dallo studio granulometrico delle polveri è relativa alla progettazione dei sistemi di protezione. Con le cautele che il caso richiede (cfr. NFPA 68) è possibile dar corso ad una valutazione preliminare dei parametri di esplosione (Kst, Pmax) attraverso un confronto granulometrico con polveri analoghe già testate16 al fine di determinarne i parametri necessari alla progettazione dei sistemi di protezione. Tale valutazione deve obbligatoriamente comprendere anche una verifica del processo di produzione dal quale le polveri hanno avuto origine; il medesimo profilo granulometrico, prodotto da processi industriali differenti, può infatti generare polveri con parametri di esplosione diversi. Questo perché le polveri con granulometria analoga possono evidenziare una disuguale forma dei grani. Forme frastagliate, a parità di profilo granulometrico, risultano maggiormente reattive rispetto a forme meno “accidentate”; è per questo motivo che oltre alla granulometria sarà necessario procedere ad un confronto del processo produttivo che ha condotto alla formazione di tali polveri17. Questa variabilità, funzione del ciclo di produzione, si annulla per diametri medi inferiori a 63 µm (Bartknecht, 1989). Al di sotto di tale valore, quindi, sarà possibile confrontare i profili granulometrici e estrapolare i parametri di esplosione senza ulteriori considerazioni. In generale, il diametro medio delle polveri possiede pertanto un valore descrittivo ma non quantitativo. Polveri con medesimo valore medio granulometrico possono manifestare caratteristiche di esplosione radicalmente diverse, anche perché è possibile siano presenti frazioni fini in quantità molto differenti. L’assunzione fatta in termini di parametri di esplosione dovrà pertanto essere successivamente validata attraverso l’esecuzione di test di esplosione specifici.
Figura 2.7 – Esempio di profilo granulometrico di una polvere combustibile
2.1.8 I parametri caratteristici di esplosione
I parametri necessari al dimensionamento dei sistemi di protezione contro le esplosioni sono ottenibili attraverso la misura di due proprietà caratteristiche: la pressione massima di esplosione (Pmax) e la caratteristica specifica di esplosione (Kg nel caso dei gas e vapori, Kst nel caso delle polveri). Quest’ultimo parametro risulta direttamente collegato alla massima velocità di incremento della pressione durante il test di esplosione (dP/dt)max, grazie alla cosiddetta legge cubica:

dove:
| K | rappresenta la caratteristica specifica di esplosione testata in condizioni di test normalizzate (Kg per gas, Kst per polveri) e misurata in [bar · m/s] |
| (dP/dt)max | è la massima velocità di incremento della pressione durante il test, misurata in [bar/s]; |
| V | è il volume nel quale è realizzato il test di esplosione, misurato in [m3]. |
La legge cubica indica che, all’aumentare del volume del contenimento all’interno del quale ha luogo l’esplosione, la velocità di incremento della pressione (e quindi la violenza della stessa) tende a diminuire in proporzione alla radice cubica del volume stesso. Tale considerazione porta con sé importanti implicazioni, soprattutto relativamente al dimensionamento dei sistemi di protezione contro le esplosioni.
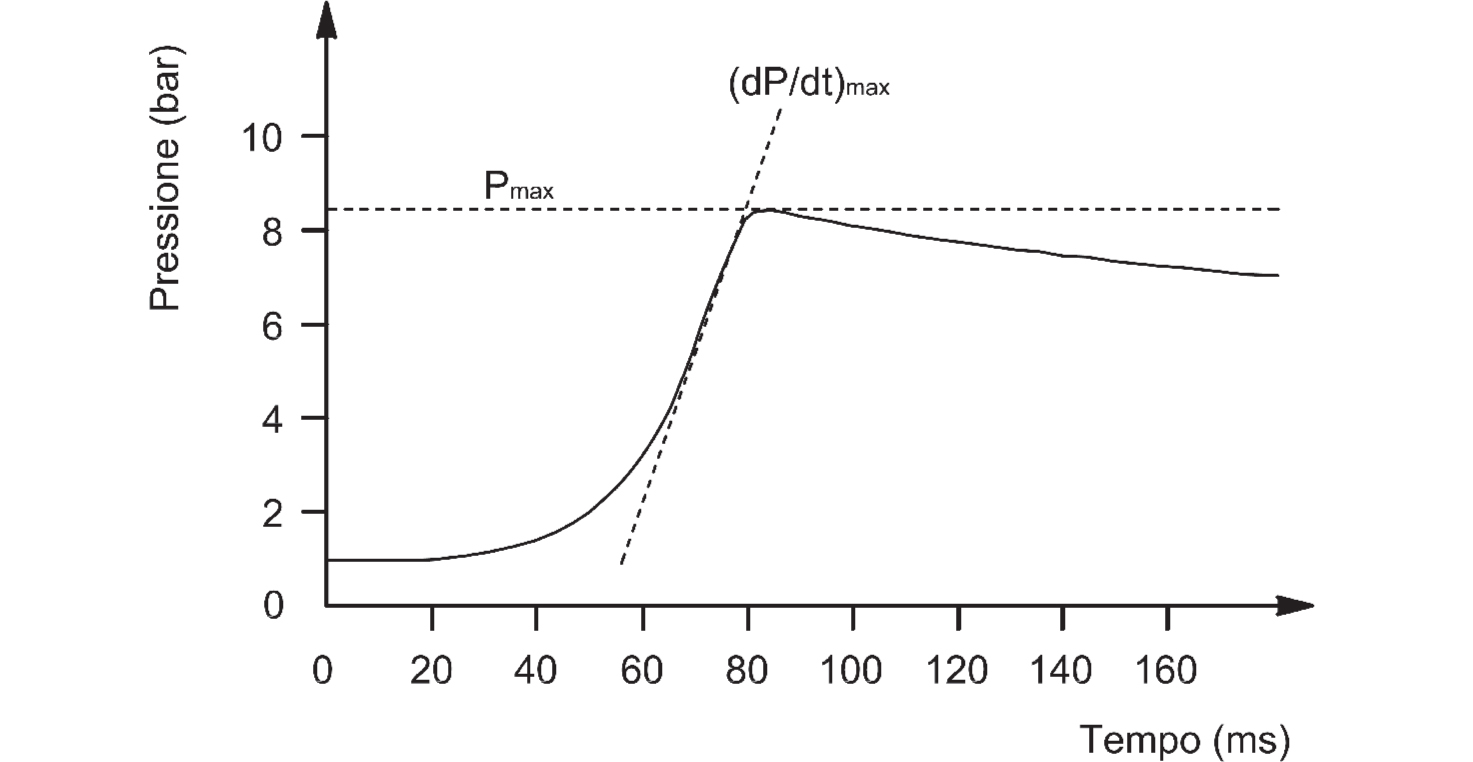
Il K uguaglia la massima velocità di incremento della pressione (dP/dt)max in corrispondenza del volume unitario di test (1 m3). Tale volume rappresenta l’ampiezza della sfera di test previsto dalla Norma (UNI EN 14034-1 e UNI EN 14034-2). È tuttavia permessa l’esecuzione di test con dispositivo di prova avente un volume di 20 litri (sfera di Siwek), che permette di ridurre notevolmente la quantità di sostanza necessaria per il test (a questo proposito si faccia riferimento al commento presente nella sezione applicativa del presente capitolo). Un esempio grafico delle relazioni descritte è illustrato in Figura 2.8, rappresentante l’andamento di un test di esplosione per gas infiammabile; in esso si identifica un valore di Pmax pari a 8,5 bar e di (dP/dt)max uguale a circa 316 bar·m/s.
Come già detto, i risultati del test si possono estendere direttamente alla protezione degli impianti industriali attraverso la legge cubica (eq. 2.12) e l’utilizzo della Normativa tecnica (NFPA 68, UNI EN 14491, UNI EN 14994). Mentre tuttavia, nel caso dei gas infiammabili, l’utilizzo dei risultati del test non determina particolari sovradimensionamenti dei sistemi di protezione, nel caso delle polveri combustibili è possibile che la prova sovrastimi le condizioni di turbolenza rispetto alla realtà dell’impianto e quindi le relative necessità di protezione (Dahoe, 2000).
Al variare delle condizioni di turbolenza nei test di gas non si verifica, infatti, una sostanziale modifica della pressione massima di esplosione Pmax mentre nelle polveri combustibili l’incremento della Pmax in funzione della turbolenza risulta particolarmente evidente (Nagy et al., 1983; Bartknecht, 1989).
Figura 2.8 – Test di esplosione con gas infiammabili
In generale, il valore di Kst dipende dalle seguenti variabili:
-
composizione delle miscela di test;
-
turbolenza nel dispositivo di test;
-
energia di accensione della miscela.
Quest’ultimo parametro risulta particolarmente delicato nell’esecuzione del test di esplosione e delle conclusioni che dalla prova derivano. Come vedremo in seguito, il dimensionamento dei sistemi di protezione è basato sui dati delle prove di esplosione eseguiti con un innesco dell’ATEX conforme alla Normativa. Sarà pertanto necessario evitare inneschi ad alta energia (Flame Jet Ignition) nel contenimento che pregiudicherebbero l’efficacia del sistema di protezione installato. Sia Kst che Kg sono quindi proprietà delle sostanze ma il loro valore dipende dalle condizioni di esecuzione del test. Il parametro Kst possiede la caratteristica di essere (sotto specifiche condizioni) invariante rispetto al volume di prova. Studi approfonditi (Bartknecht, 1989) hanno infatti dimostrato l’invarianza di tale parametro in test di esplosione realizzati in volumi variabili da 0,02 m3 a 10 m3. Il Kg risulta invece volume dipendente e non può essere considerato costante (NFPA 68).
Nell’ipotesi in cui non sia noto il Kg di un gas infiammabile, è possibile determinarne comunque il valore (orientativo) grazie alla conoscenza del Kg di un altro gas infiammabile (note che siano le velocità di combustione laminare di entrambi) attraverso la seguente equazione:

dove Su è la velocità di combustione laminare.
Nel caso delle polveri combustibili, in assenza di dati relativi al Kst si può ricorrere ad una relazione approssimata, calcolata a partire dalla velocità di combustione turbolenta St e dal Pmax (Abbasi et al., 2007) come indicato in eq. 2.14:
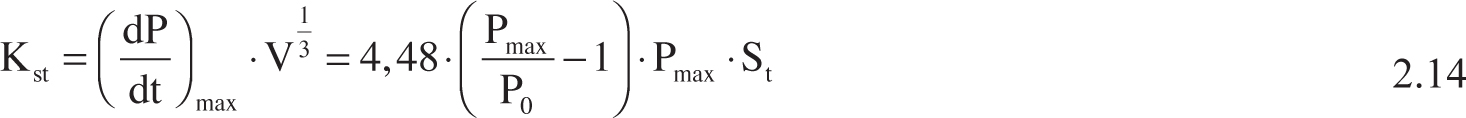
Con le polveri combustibili, i parametri di esplosione si riducono all’aumentare del diametro medio. In particolare nel caso delle più comuni polveri organiche (Figura 2.9), si rileva un azzeramento dei parametri misurati per diametri medi superiori a circa 400 µm. A seguito di tale considerazione il CEN assume esplosive tutte le polveri combustibili aventi frazioni granulometriche significative minori di 500 µm (420 µm per NFPA)18. Tale assunzione risulta probabilmente molto conservativa; nel caso di Figura 2.9 il PVC in polvere, per esempio, annulla i parametri di esplosione già per diametri superiori a 250 µm. Inoltre la velocità massima di incremento, rappresentativa della violenza dell’esplosione, tende ad annullarsi già a partire da valori di granulometria superiori a 300 µm, indipendentemente dal tipo di polvere testato.
Figura 2.9 – Effetti del valor medio sui parametri di esplosione per alcune polveri organiche
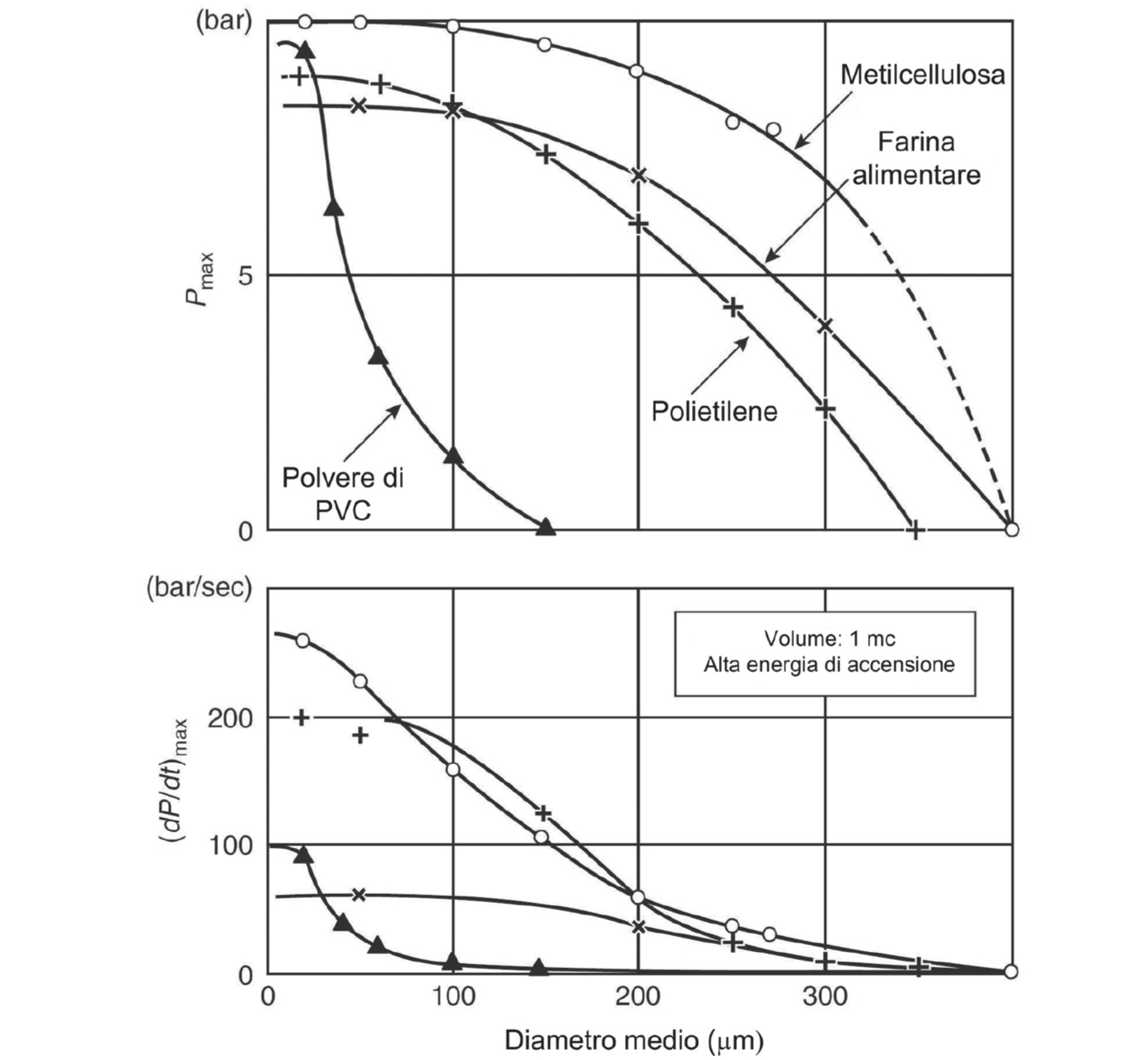
Fonte: NFPA Handbook, 2001
I parametri esplosione tendono inoltre a diminuire al diminuire della concentrazione di ossigeno, azzerandosi al di sotto del LOC. Questa considerazione mantiene la propria validità sia nel caso di gas e vapori infiammabili sia nel caso delle polveri combustibili. In particolare (Eckhoff, 2004), i parametri di esplosione nel caso di ATEX dovute a polveri variano, al variare della concentrazione di O2, secondo le seguenti relazioni:


Con evidente significato dei simboli.
Nel caso in cui i parametri di esplosione siano necessari al calcolo dei sistemi di protezione in impianti con ATEX causata da polveri combustibili, una particolare attenzione dovrà essere posta all’estrazione di un campione realmente significativo della granulometria trattata nell’impianto. All’interno degli impianti le polveri che si mantengono in sospensione sono le più sottili. In genere, infatti, la velocità di sedimentazione del particolato è una funzione diretta del diametro; maggiore è il calibro della particella, maggiore sarà la sua velocità di sostentamento (Figura 2.10).
Pertanto la presenza di turbolenze modeste all’interno degli impianti (es. silos), contribuisce a mantenere sospese solo le frazioni granulometriche più fini dato che le altre, essendo la velocità insufficiente, tenderanno a depositarsi sul fondo.
Un’ulteriore problematica, in tale senso, è legata alla progressiva riduzione granulometrica all’interno dell’impianto. La polvere sulla quale si eseguiranno i test dovrà essere quindi tale da rappresentare le reali condizioni operative dell’impianto (Cardillo, 2002). Assumono rilevanza, nella scelta della polvere rappresentativa, i seguenti parametri:
-
polvere fine;
-
campioni estratti di recente;
-
campioni macinati;
-
campioni essiccati.
La pericolosità della polvere è suddivisa in classi secondo quanto indicato in Tabella 2.11; tale classificazione risulta particolarmente importante per definire i limiti di applicazione delle varie strategie di protezione degli impianti.
Figura 2.10 – Velocità di sedimentazione in funzione del diametro delle particelle
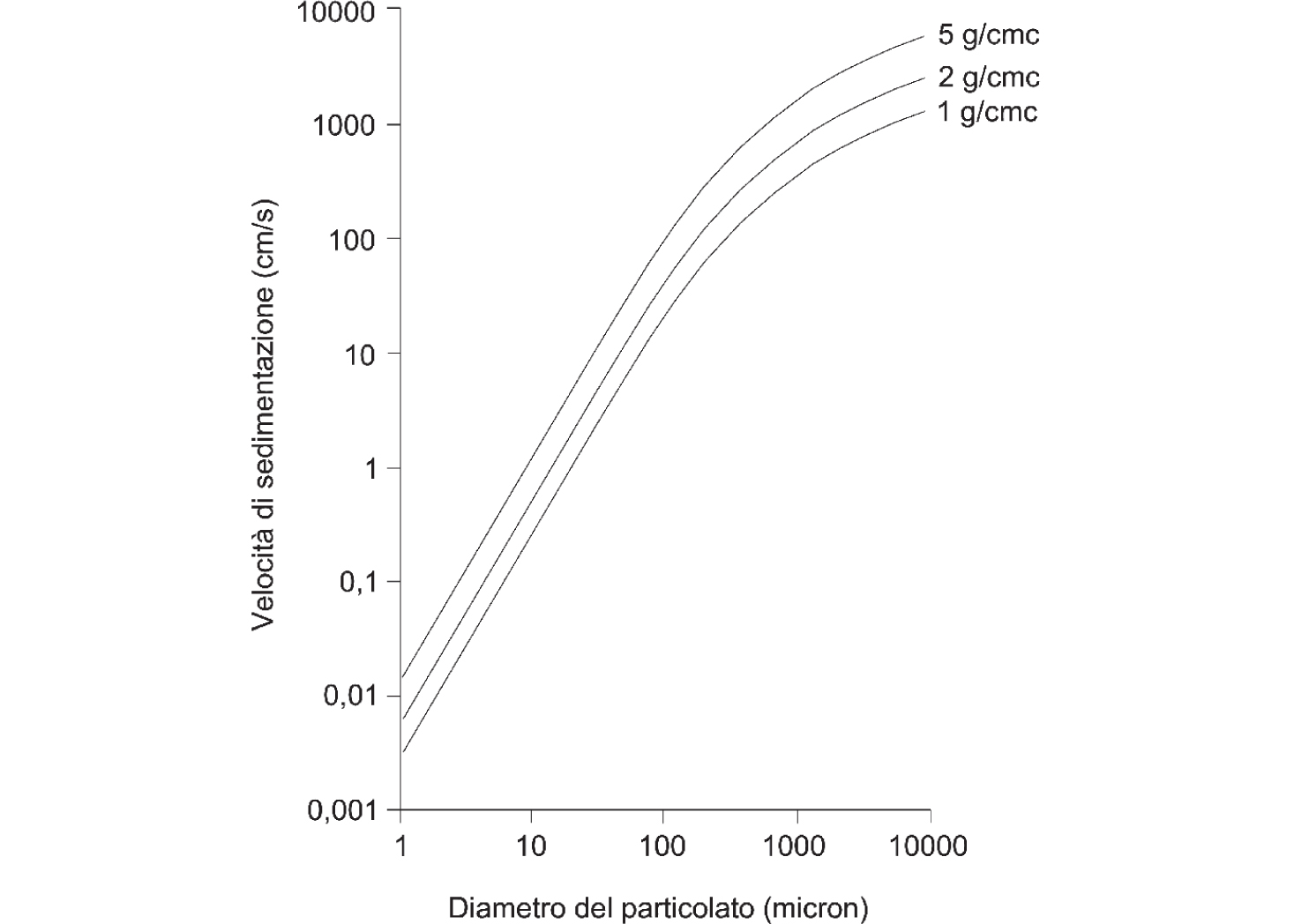
Fonte: INERIS, 2001
Tabella 2.11 – Classi di pericolo per le polveri combustibili
| Classe della polvere | Kst (bar∙m/s) | Pmax (bar) |
|---|---|---|
| St1 | ≤ 200 | 10 |
| St2 | 201-300 | 10 |
| St3 | > 300 | 12 |
Le caratteristiche di esplosione, nel caso di polveri miscelate con liquidi infiammabili, manifestano dapprima una diminuzione dei parametri misurati a causa dell’effetto agglomerante dei liquidi stessi sulle polveri. Superata una data concentrazione di solvente, tali caratteristiche riprendono ad aumentare a causa della massiva formazione di vapori di solvente.
Nel caso dell’etanolo, per esempio, la concentrazione limite si colloca attorno al 25%, mentre nel caso dell’acetone si posiziona attorno a valori inferiori al 10% a causa dell’elevata volatilità di quest’ultimo.
2.1.9 Le caratteristiche di caricamento elettrostatico
Un altro fondamentale parametro necessario alla valutazione prevista dal titolo XI del D.Lgs. n. 81/2008 riguarda l’attitudine dei materiali (gas, liquidi, solidi) a caricarsi elettrostaticamente. Tale aspetto pur essendo indipendente dall’infiammabilità della sostanza analizzata deve essere tenuto in considerazione nella valutazione del rischio di accensione elettrostatica, come vedremo nel seguito del testo (Capitolo 6). Definendo la resistività in volume come la resistenza di un corpo di sezione e resistenza unitarie, la linea guida CLC/TR 60079-32-1 classifica i liquidi con costante dielettrica pari a circa 2 in tre categorie di conducibilità (definita come l’inverso della resistività in volume):
-
alta conducibilità (es. alcoli, chetoni, acqua bidistallata, acqua non distillata, glicole e glicoletere): si verifica con valori superiori a 10000 pS/m;
-
media conducibilità (es. combustibili e oli contenenti additivi dissipativi, oli combustibili pesanti, esteri): si verifica tra 10000 pS/m e 50 pS/m;
-
bassa conducibilità (es. paraffine altamente depurate, toluene, benzina, gasolio, eteri eccetto glicole): si verifica in corrispondenza di valori inferiori a 50 pS/m.
A titolo illustrativo, si riportano in Tabella 2.12 i dati di resistività di alcuni liquidi infiammabili particolarmente significativi.
Tabella 2.12 – Conducibilità, tempi di riposo e classificazione di alcuni liquidi infiammabili
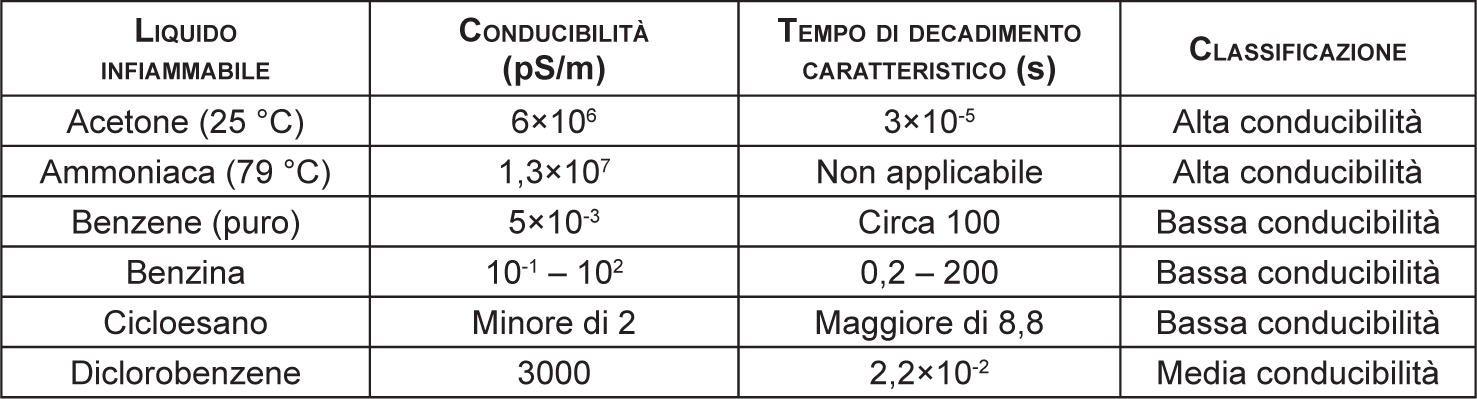
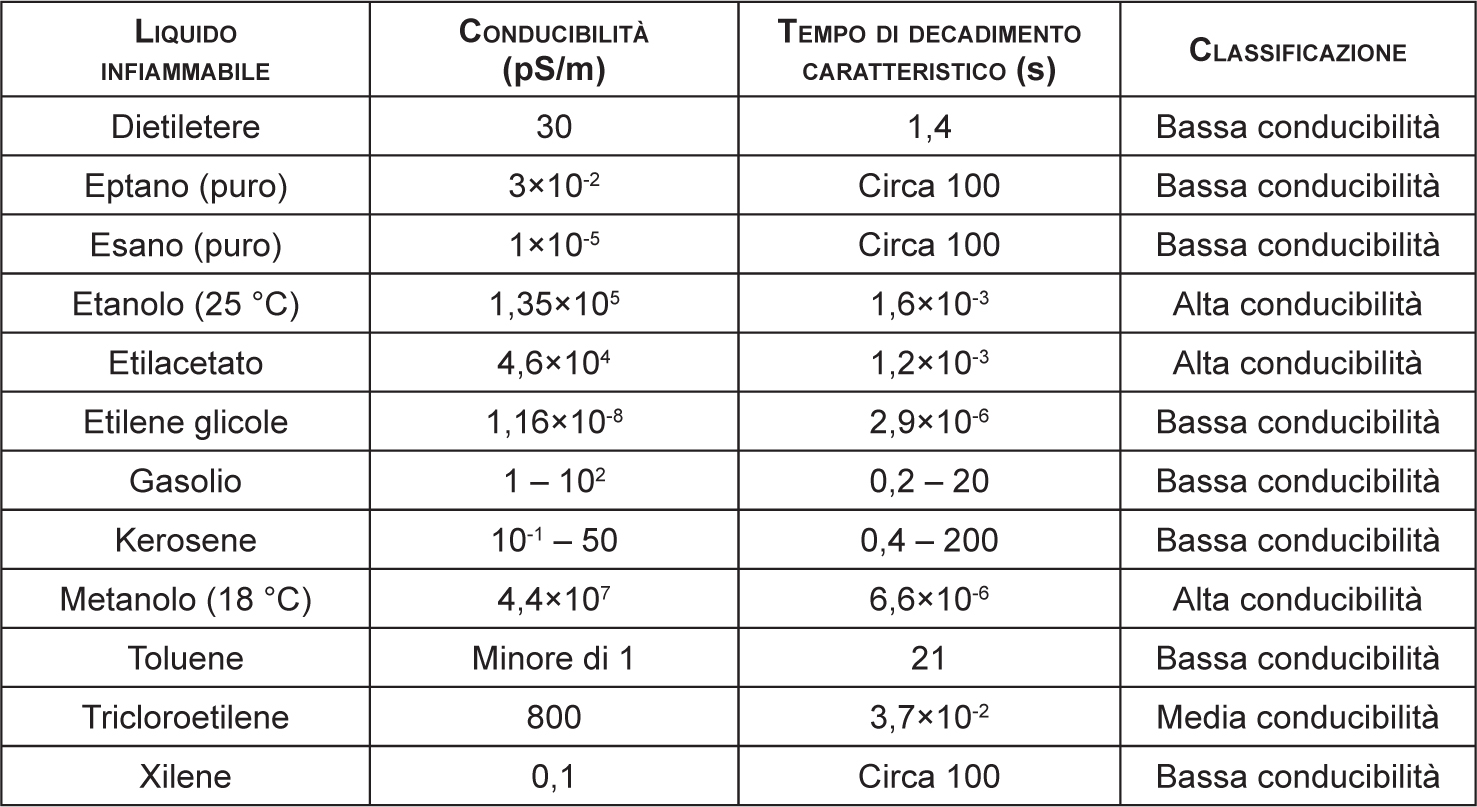
Fonte: NFPA 77, CLC/TR 60079-32-1
In assenza di generazione di cariche, la densità di carica nel liquido diminuisce secondo una legge esponenziale di decadimento. Nel tempo di decadimento caratteristico la carica si riduce a circa 1/e (circa il 37%) del suo valore originale.
La stessa Norma CLC/TR 60079-32-1 classifica, inoltre, l’attitudine al caricamento elettrostatico dei solidi (polveri) in funzione della resistività in volume secondo la seguente regola:
-
bassa resistività di volume (Le polveri ad alta resistività sono rare. Anche le polveri metalliche, un tempo ritenute tali, non restano conduttive per molto tempo poiché formano in breve tempo film ossidanti e/o passivi sulla loro superficie che contribuiscono ad aumentare la resistenza. Il carbone ed il coke metallurgico rientrano invece in questa categoria): si verifica con resistività di volume fino a 106 Ωm;
-
media resistività di volume (es. molte polveri organiche naturali): si verifica con resistività di volume compresa tra 106 Ωm e 1010 Ωm;
-
alta resistività di volume (es. polimeri, alcune polveri organiche sintetiche e polveri organiche naturali molto secche): si verifica con resistività di volume uguale o superiore a 1010 Ωm.
Alcuni valori di resistività di volume relativi a polveri specifiche, sono riportati in Tabella 2.13.
Le norme per l’esecuzione dei test di conducibilità e resistività sono la DIN 51412 (conducibilità di liquidi e sospensioni) e la ASTM D257 e IEC 1241-2-2 (resistività di volume per polveri) oltre alla CEI EN 60079-32-2.
La determinazione dei parametri di resistività risulta essenziale per definire il grado di caricamento elettrostatico delle sostanze coinvolte nel processo produttivo e quindi valutare l’efficacia degli inneschi elettrostatici delle ATEX eventualmente presenti nel ciclo di produzione.
2.1.10 Le incompatibilità tra le sostanze
In molti casi l’esplosione risulta ascrivibile non già alla sola presenza di una sostanza infiammabile, quanto alla sua reattività con altre sostanze/miscele/materiali. Questo aspetto, pur se di pertinenza specifica della valutazione di rischio chimico (cfr. Titolo IX, D.Lgs. n. 81/2008) deve comunque essere tenuto in debita considerazione anche nell’ambito della formazione di ATEX. In questo senso, un importante strumento di analisi, messo a disposizione dal NOAA19 Statunitense, è il software CAMEO Chemicals il quale fornisce una serie di aggiornate informazioni relative alla compatibilità incrociata tra sostanze20.
Figura 2.11 – Schermata iniziale del software CAMEO Chemicals
A titolo riepilogativo, si riportano in Tabella 2.13 i profili di reattività delle sostanze infiammabili elencate in Tabella 2.18, così come presentati in CAMEO Chemicals.
Tabella 2.13 – Profili di reattività delle sostanze descritte in Tabella 2.12
| Sostanza | Profilo di reattività |
|---|---|
| Acetone (Acetone) | It was reported that a mixture of ACETONE and chloroform, in a residue bottle, exploded. Since addition of acetone to chloroform in the presence of base will result in a highly exothermic reaction, it is thought that a base was in the bottle [MCA Case History 1661, 1970]. Also, Nitrosyl chloride, sealed in a tube with a residue of acetone in the presence of platinum catalyst, gave an explosive reaction [Chem. Eng. News 35(43):60, 1967]. The reaction of nitrosyl perchlorate and acetone ignites and explodes. Explosions occur with mixtures of nitrosyl perchlorate and primary amine [Ann. Chem. 42:2031, 1909]. Reacts violently with nitric acid. Also causes exothermic reaction when in contact with aldehydes. |
| Sostanza | Profilo di reattività |
|---|---|
| Acetilene (Acetylene) | ACETYLENE reacts with alkali metals, forming Hydrogen gas. Acetylene can react explosively with bromine [Von Schwartz 1918, p. 142]. Acetylene forms a sensitive acetylide when passed into an aqueous solution of mercuric nitrate, [Mellor 4:933, 1946-47]. An acetylene torch used to drill through a plow frame, which was filled with hydrogen gas, produced an explosion [NIOSH, June 1998]. It reacts with silver, copper and lead to form sensitive, explosive salts. Since acetylene is endothermic and effectively a reducing agent, it’s reaction with oxidants can be very violent (examples: calcium hypochlorite, nitric acid, nitrogen oxide, ozone, trifluoromethyl hypofluorite, etc.). Contact of very cold liquefied gas with water may result in vigorous or violent boiling of the product and extremely rapid vaporization, due to the large temperature differences involved. If the water is hot, there is the possibility that a liquid “superheat” explosion may occur. |
| Acetilene (Acetylene) | Pressures may build to dangerous levels if liquid gas contacts water in a closed container [Handling Chemicals Safely 1980]. Acetylene and ammonia can form explosive silver salts in contact with Ag. (Renner, Hermann, Gunther Schlamp. “Silver, Silver Compounds, and Silver Alloys.” Ullmann’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA, 2001). |
| Ammoniaca anidra (Ammonia anhydrous) | AMMONIA is a base. Reacts exothermically with all acids. Violent reactions are possible. Readily combines with silver oxide or mercury to form compounds that explode on contact with halogens. When in contact with chlorates it forms explosive ammonium chlorate [Kirk-Othmer, 3rd ed., Vol. 2, 1978, p. 470]. Reacts violently or produces explosive products with fluorine, chlorine, bromine and iodine and some of the interhalogen compounds (bromine pentafluoride, chlorine trifluoride). Mixing of bleaching powder (hypochlorite solution) with ammonia solutions produces toxic/explosive ammonia trichloride vapors. Undergoes potentially violent or explosive reactions on contact with 1,2-dichloroethane (with liquid ammonia), boron halides, ethylene oxide (polymerization), perchlorates or strong oxidants (chromyl chloride, chromium trioxide, chromic acid, nitric acid, hydrogen peroxide, chlorates, fluorine, nitrogen oxide, liquid oxygen). Reacts with silver chloride, silver oxide, silver nitrate or silver azide to form the explosive silver nitride. May react with some heavy metal compounds (mercury, gold(III) chloride) to produce materials that may explode when dry. [Bretherick, 5th ed., 1995, p. 1553]. |
| Benzene (Benzene) | BENZENE reacts vigorously with allyl chloride or other alkyl halides even at minus 70 °C in the presence of ethyl aluminum dichloride or ethyl aluminum sesquichloride. Explosions have been reported [NFPA 491M 1991]. Ignites in contact with powdered chromic anhydride [Mellor 11:235, 1946-47]. Incompatible with oxidizing agents such as nitric acid. Mixtures with bromine trifluoride, bromine pentafluoride, iodine pentafluoride, iodine heptafluoride and other interhalogens can ignite upon heating [Bretherick 5th ed. 1995]. Benzene and cyanogen halides yield HCl as a byproduct (Hagedorn, F. H. Gelbke, and Federal Republic of Germany, 2002, Nitriles. In Ullman’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA). The reaction of benzene and trichloroacetonitrile evolves toxic chloroform and HCl gasses. (Hagedorn, F., H.-P. Gelbke, and Federal Republic of Germany. 2002. Nitriles. In Ullman’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA). |
| Butano (Butane) | BUTANE can explode when exposed to flame or when mixed with (nickel carbonyl + oxygen). It can also react with oxidizers. Strong acids and alkalis should be avoided. (NTP, 1992). |
| Cicloesano (Cyclohexane) | Liquid nitrogen dioxide was fed into a nitration column containing hot CYCLOHEXANE, due to an error. An explosion resulted [MCA Case History 128(1962)] Incompatible with strong oxidizers. |
| Sostanza | Profilo di reattività |
|---|---|
| Dietiletere (Diethyl Ether) | Occasional explosions have occurred when aluminum hydride was stored in ether. The explosions have been blamed on the presence of carbon dioxide impurity in the ether, [J. Amer. Chem. Soc. 70:877(1948)]. Diethyl ether and chromium trioxide react violently at room temperature. Solid acetyl peroxide in contact with ether or any volatile solvent may explode violently. A 5-gram portion in ether detonated while being carried, [Chem. Eng. News 27:175(1949)]. Nitrosyl perchlorate ignites and explodes with diethyl ether. A mixture of ether and ozone forms aldehyde and acetic acid and a heavy liquid, ethyl peroxide, an explosive, [Mellor 1:911(1946-1947)]. |
| Eptano (Heptane) | HEPTANE is incompatible with the following: Strong oxidizers (NIOSH, 1997). |
| Etano (Ethane) | Saturated aliphatic hydrocarbons, such as ETHANE, may be incompatible with strong oxidizing agents like nitric acid. Charring of the hydrocarbon may occur followed by ignition of unreacted hydrocarbon and other nearby combustibles. In other settings, aliphatic saturated hydrocarbons are mostly unreactive. They are not affected by aqueous solutions of acids, alkalis, most oxidizing agents, and most reducing agents. Peroxidizable. |
| Etanolo (Ethyl Alcohol) | ETHANOL reacts violently with acetyl chloride and acetyl bromide [Rose, (1961); Merck 11th ed., 1989]. Mixtures with concentrated sulfuric acid and strong hydrogen peroxide can cause explosions. Mixtures with concentrated hydrogen peroxide form powerful explosives. Reacts readily with hypochlorous acid and with chlorine to give ethyl hypochlorite, which decomposes in the cold and explodes on exposure to sunlight or heat. Base-catalysed reactions with isocyanates should be carried out in inert solvents. Such reactions in the absence of solvents often occur with explosive violence [Wischmeyer(1969)]. Highly oxidized potassium metal was dropped into a dish of ethyl alcohol, an immediate explosion shattered the dish. Potassium superoxide was considered the cause of the reaction [Health and Safety Inf. 251(1967)]. Ethanol or methanol can ignite on contact with a platinum-black catalyst. (Urben 1794). |
| Etilacetato (Ethyl Acetate) | ETHYL ACETATE is also sensitive to heat. On prolonged storage, materials containing similar functional groups have formed explosive peroxides. This chemical may ignite or explode with lithium aluminum hydride. It may also ignite with potassium tert-butoxide. It is incompatible with nitrates, strong alkalis and strong acids. It will attack some forms of plastics, rubber and coatings. It is incompatible with oxidizers such as hydrogen peroxide, nitric acid, perchloric acid and chromium trioxide. Violent reactions occur with chlorosulfonic acid. (NTP, 1992). SOCl2 reacts with esters, such as ethyl acetate, forming toxic SO2 gas and water soluble/toxic acyl chlorides, catalyzed by Fe or Zn (Spagnuolo, C.J. et al. 1992. Chemical and Engineering News 70(22):2.). |
| Etilene (Ethylene) | Peroxidizable monomer may initiate exothermic polymerization of the bulk material [Bretherick 1979, p. 160]. Ethylene in the presence of aluminum chloride may undergo a violent reaction [J. Inst. Pet. 33:254. 1947]. Ozone and ethylene react explosively [Berichte 38:3837]. Ethylene can polymerize at low pressure if catalyzed by titanium halides. (Sundaram, K. M, M. M. Shreehan, E. F. Olszewski. “Ethylene.” Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. 2001.) |
| Esano Hexane) | HEXANE may be sensitive to light. It may also be sensitive to prolonged exposure to heat. This compound can react vigorously with oxidizing materials. This would include compounds such as liquid chlorine, concentrated O2, sodium hypochlorite and calcium hypochlorite. It is also incompatible with dinitrogen tetraoxide. It will attack some forms of plastics, rubber and coatings. (NTP, 1992). |
| Sostanza | Profilo di reattività |
|---|---|
| Idrogeno (Hydrogen) | Finely divided platinum and some other metals will cause a mixture of hydrogen and oxygen to explode at ordinary temperatures. If a jet of hydrogen in air impinges on platinum black the metal surface gets hot enough to ignite the gases, [Mellor 1:325(1946-1947)]. Explosive reactions occur upon ignition of mixtures of nitrogen trifluoride with good reducing agents such as ammonia, hydrogen, hydrogen sulfide or methane. Mixtures of hydrogen, carbon monoxide, or methane and oxygen difluoride are exploded when a spark is discharged, [Mellor 2, Supp. 1:192(1956)]. An explosion occurred upon heating 1’-pentol and 1”-pentol under hydrogen pressure. It appears that this acetylenic compound under certain conditions suddenly breaks down to form elemental carbon, hydrogen, and carbon monoxide with the release of sufficient energy to develop pressures in excess of 1000 atmospheres, [AIChE Loss Prevention, p. 1, (1967)]. |
| Metano (Methane) | METHANE is a reducing agent, it is involved in many explosions when combined with especially powerful oxidizers such as bromine pentafluoride, chlorine trifluoride, chlorine, iodine, heptafluoride, dioxygenyl tetrafluoroborate, dioxygen difluoride, trioxygen difluoride and liquid oxygen. Other violent reactions include, chlorine dioxide and nitrogen trifluoride. Liquid oxygen gives an explosive mixture when combined with liquid methane [NFPA 1991]. Contact of very cold liquefied gas with water may result in vigorous or violent boiling of the product and extremely rapid vaporization due to the large temperature differences involved. If the water is hot, there is the possibility that a liquid “superheat” explosion may occur. Pressures may build to dangerous levels if liquid gas contacts water in a closed container [Handling Chemicals Safely 1980]. |
| Metanolo (Methyl alcohol) | METHANOL reacts violently with acetyl bromide [Merck 11th ed. 1989]. Mixtures with concentrated sulfuric acid and concentrated hydrogen peroxide can cause explosions. Reacts with hypochlorous acid either in water solution or mixed water/carbon tetrachloride solution to give methyl hypochlorite, which decomposes in the cold and may explode on exposure to sunlight or heat. Gives the same product with chlorine. Can react explosively with isocyanates under basic conditions. The presence of an inert solvent mitigates this reaction [Wischmeyer 1969]. A violent exothermic reaction occurred between methyl alcohol and bromine in a mixing cylinder [MCA Case History 1863. 1972]. A flask of anhydrous lead perchlorate dissolved in methanol exploded when it was disturbed [J. Am. Chem. Soc. 52:2391. 1930]. P4O6 reacts violently with methanol. (Thorpe, T. E. et al., J. Chem. Soc., 1890, 57, 569-573). Ethanol or methanol can ignite on contact with a platinum-black catalyst. (Urben 1794). |
| Monossido di Carbonio (Carbon Monoxide) | Bromine trifluoride and carbon monoxide react explosively at high temperatures or concentrations [Mellor 2 Supp. 1:166 1956]. The same is true for various oxidizers such as: chlorine dioxide, oxygen (liquid), peroxodisulfuryl difluoride. The product of the reaction between lithium and carbon monoxide, lithium carbonyl, detonates violently with water, igniting the gaseous products [Mellor 2, Supp. 2:84, 1961]. Potassium and sodium metals behave similarly. Cesium oxide, iron(III) oxide, and silver oxide all react, in the presence of moisture, at ambient temperatures with carbon monoxide causing ignition, [Mellor, 1941, vol. 2, 487]. Contact of very cold liquefied gas with water may result in vigorous or violent boiling of the product and extremely rapid vaporization due to the large temperature differences involved. If the water is hot, there is the possibility that a liquid “superheat” explosion may occur. Pressures may build to dangerous levels if liquid gas contacts water in a closed container [Handling Chemicals Safely 1980]. |
| Pentano (Pentane) | N-PENTANE is incompatible with strong oxidizers. It is also incompatible with strong acids, alkalis, and oxygen. Mixtures with chlorine gas have produced explosions. It will attack some forms of plastics, rubber, and coatings. (NTP, 1992) |
| Propano (Propane) | PROPANE is incompatible with strong oxidizing agents. |
| Sostanza | Profilo di reattività |
|---|---|
| Toluene (Toluene) | TOLUENE reacts vigorously with allyl chloride or other alkyl halides even at minus 70° C in the presence of ethyl aluminum dichloride or ethyl aluminum sesquichloride. Explosions have been reported [NFPA 491M 1991]. Incompatible with strong oxidizing agents. When added to a tank of sulfur dichloride, the tank over pressurized and ruptured in a reaction thought to be catalyzed by iron or iron(III) chloride [Chem. Eng. News, 1988, 66(32), 2]. |
| Xilene (Xylene) | XYLENE reacts exothermically with sulfuric acid, nitric acid, and strong oxidizing agents [Handling Chemicals Safely 1980, p. 962]. |
Fonte: CAMEO Chemicals, Version 2.3
2.1.11 Test di combustibilità delle polveri
Questo test, da realizzarsi in conformità alla Norma VDI 2263-1, verifica se, e in quale misura, un incendio innescato da una fonte di accensione esterna possa propagarsi nel campione di polvere appositamente preparato. Preliminarmente, quindi, viene stesa una striscia di polvere combustibile, avente sezione triangolare lunga 20 cm, larga 4 cm e alta 2 cm, su di una base realizzata in ceramica.
Ad una estremità si esegue un tentativo di innesco della combustione con un filo in platino incandescente avente una temperatura superficiale pari a circa 1000 °C. Il filo viene immerso solo brevemente nel campione in polvere, in modo che quest’ultimo non possa essere riscaldato.
Figura 2.12 – Test di combustibilità (VDI 2263-1)
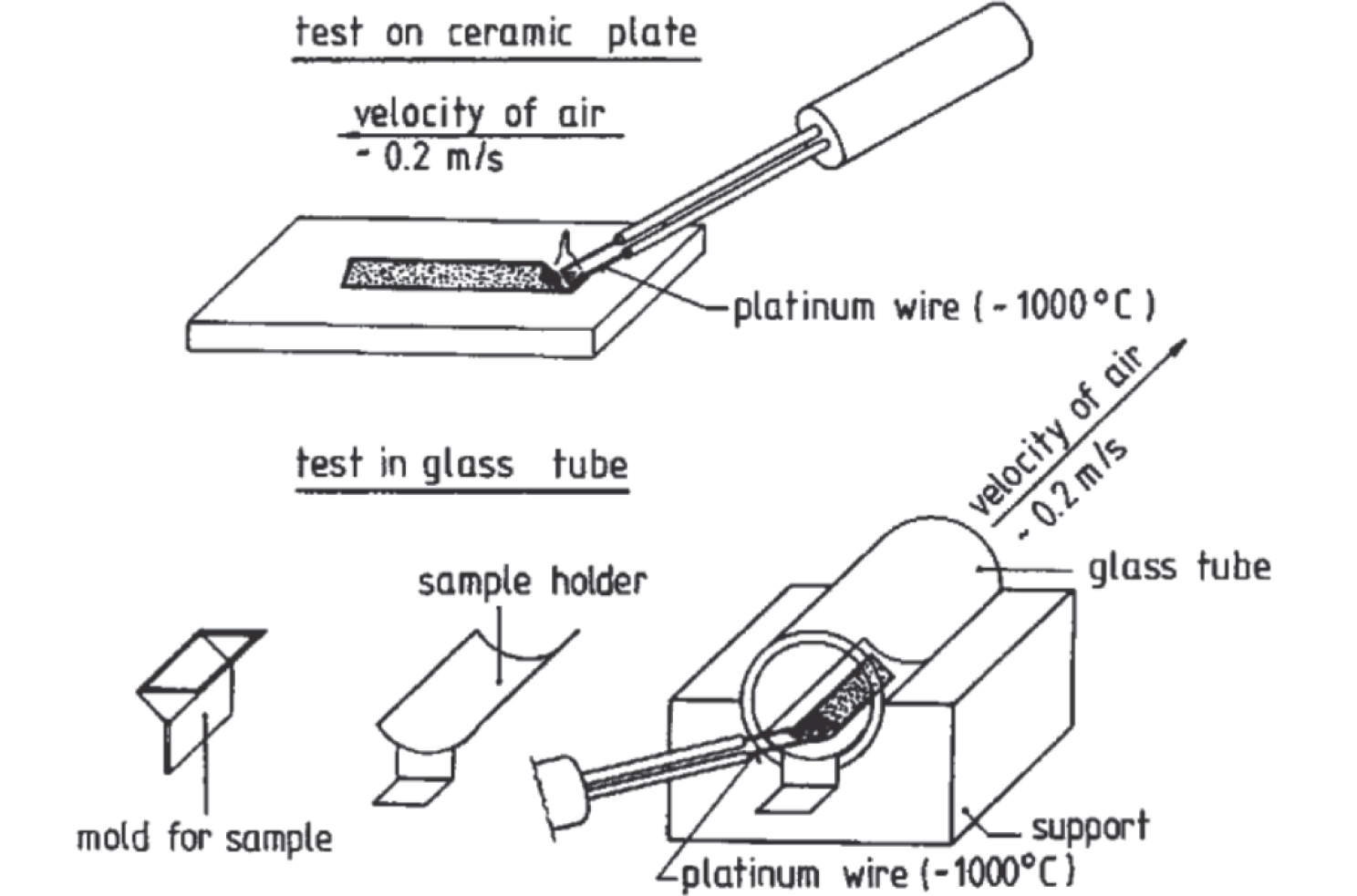
Nel caso di fusione della sostanza, il test subisce una modifica consistente con l’aggiunta alle polveri del 20% in peso di farina fossile. Tale addizione impedisce, nella maggioranza dei campioni, la fusione.
L’attitudine all’infiammabilità è valutata con un indice BZ che va da 1 a 6 secondo quanto indicato in Tabella 2.14.
Tabella 2.14 – Criteri di combustibilità delle polveri (VDI 2263-1)
| Tipo di reazione | Classe BZ | Esempi di materiali | |
|---|---|---|---|
| Assenza di propagazione delle fiamme | Nessuna accensione | 1 | Sale da tavola, Acido stearico (1300 µm) |
| Breve accensione e rapido spegnimento | 2 | Acido tartarico, polipropilene (162 µm) | |
| Combustione o incandescenza localizzata senza praticamente propagazione | 3 | Polipropilene (25 µm) | |
| Propagazione delle fiamme | Incandescenza senza scintille (senza fiamma) o lenta decomposizione senza fiamma | 4 | Resina fenolo-formaldeide (60 µm) |
| Combustione con fiamma o generazione di scintille | 5 | Zolfo, Metilcellulosa (29 µm) | |
| Combustione molto rapida con propagazione delle fiamme o rapida decomposizione senza fiamma | 6 | Polvere nera, Calcio/Alluminio (22 µm) | |
2.1.12 Test di screening di esplodibilità (US Bureau of Mines Report of Investigations 5624, Laboratory Equipment and Test Procedure for Evaluating Explosibility of Dusts)
Il test di screening è volto a classificare l’esplodibilità di una nube di polvere; esso è finalizzato a determinare se essa può esplodere quando esposta ad una fonte di accensione sufficientemente energetica. I risultati in uscita dal test classificheranno la polvere come esplosiva o non esplosiva. In buona sostanza, questo test risponde alla domanda: Può questa polvere combustibile esplodere?
Il test di classificazione di esplodibilità si svolge generalmente in un tubo Hartmann modificato. L’apparecchio è costituito da un tubo verticale della capacità di 1,2 litri è montato su un sistema di dispersione della polvere. Quantità diverse di campioni di polvere sono disperse all’interno del tubo al fine di verificare l’accendibilità della nube attraverso una sorgente elettrica che garantisce un’energia pari a 10 J di innesco. Se la polvere non si accende nel tubo di Hartmann modificato, allora la sperimentazione continua nella sfera di Siwek da 20 litri con la medesima sorgente di accensione.
2.1.13 Polveri combustibili e scelta dei metodi di prova
In molte situazioni di valutazione dei rischi ATEX si pone il problema di quale tipo di test effettuare per poter raggiungere delle conclusioni in tema di esplosività o meno delle polveri (per i gas ed i liquidi infiammabili la situazione è più semplice da valutare). A questo si aggiunga il fatto che uno screening completo di test può risultare particolarmente gravoso da un punto di vista economico, soprattutto nei casi delle PMI. Il metodo che qui si propone possiede il vantaggio di risultare particolarmente rapido e con un limitato impatto economico soprattutto nei casi in cui le polveri si rivelino non combustibili. La situazione diviene ovviamente più articolata nel caso di dimostrazione della combustibilità delle polveri.
La fasi di valutazione saranno dunque le seguenti:
-
analisi volte a dimostrare la non combustibilità delle polveri;
-
analisi specifiche di esplosione, nel caso di polveri combustibili.
La non combustibilità delle polveri è dimostrabile attraverso l’esecuzione di un test granulometrico unito ad un test di combustibilità BZ. Nel caso in cui la granulometria si dimostri integralmente superiore a 0,5 mm oppure, se inferiore a tale valore, il BZ sia pari ad 1, si può concludere l’esclusione delle polveri dal campo applicativo del Titolo XI, D.Lgs. n. 81/2008 (con le accortezze che di seguito illustreremo).
Non necessariamente, infatti, una polvere inerte in strato lo è pure in nube. È possibile, infatti, che la polvere in strato non bruci a causa della presenza di sostanze inertizzanti oppure, ancora, a causa della presenza di frazioni granulometriche che tendono a rendere complessivamente inerte l’intera massa polverosa depositata. La situazione in nube può tuttavia mutare radicalmente dato che, soprattutto nei sistemi di contenimento, le polveri tendono a selezionarsi aeraulicamente ed è quindi possibile che le polveri inertizzanti presenti non permangano in sospensione in nube. Pertanto, ad integrazione di quanto suggerito in precedenza, in presenza di granulometrie ATEX e con la verifica di non combustibilità che evidenzia un BZ = 1, sarà opportuno sincerarsi dei seguenti ulteriori fattori:
-
il materiale costituente la polvere sia omogeneo e appartenente ad una sola specie chimica;
-
il profilo granulometrico manifesti un andamento unimodale;
-
la deviazione standard associata alla granulometria sia sufficientemente limitata.
Queste tre condizioni, unitamente alla non combustibilità dello strato sono sufficienti ad rendere poco probabile la genesi di un’esplosione della nube di polvere. Ovviamente tali parametri dovranno essere vagliati da uno specialista il quale, conoscendo il dettaglio del processo e nell’ambito della propria responsabilità professionale, dichiarerà la polvere “credibilmente non ATEX”. Rimane inteso che la certezza tecnica di “non esplosività” del campione la si può raggiungere solo con la batteria di test estesa elencata in Tabella 2.15. Bartknecht (1996), a questo proposito, sottolinea l’importanza di ricordare che la polvere fine può essere creata con l’abrasione di una porzione di polvere grossolana. Se è questo il caso, va riconosciuto che una mescolanza di polveri sottili, per esempio del 10% nel caso di metilcellulosa, o del 5% per il polietilene, potrebbe essere sufficiente a rendere l’intera miscela ATEX. Non esiste, cioè, un livello di concentrazione inferiore chiaramente definito per la polvere fine all’interno della polvere grossolana al di sotto della quale non debbano essere prese in considerazione misure protettive. Ma un pericolo di esplosione è potenzialmente sempre presente se il contenuto della polvere fine nel materiale grezzo e non esplosivo supera il LEL.
Tabella 2.15 – Test di esplosioni richiesti per alcuni specifici apparecchi/contenimenti
| Unità operativa | Combustibilità | Screening di esplosività | MIE | Tcl | T5mm | Kst Pmax | LOC | LEL | Resistività in volume | Caricabilità elettrostatica | Reazioni esotermiche |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Caricamento manuale | ☑ | ☑ | ☑ | ☐ | ☐ | ☐ | ☐ | ☐ | ☑ | ☑ | ☐ |
| Vagliatura, screening | ☑ | ☑ | ☑ | ☐ | ☐ | ☐ | ☐ | ☐ | ☑ | ☑ | ☐ |
| Miscelatore a doppio cono | ☑ | ☑ | ☑ | ☐ | ☐ | ☑ | ☑ | ☐ | ☑ | ☑ | ☐ |
| Miscelatore a lame | ☑ | ☑ | ☑ | ☑ | ☑ | ☐ | ☐ | ☐ | ☑ | ☑ | ☐ |
| Molino | ☑ | ☑ | ☑ | ☑ | ☑ | ☑ | ☑ | ☐ | ☑ | ☑ | ☑ |
| Micronizzatore | ☑ | ☑ | ☑ | ☐ | ☐ | ☑ | ☑ | ☐ | ☑ | ☑ | ☐ |
| Essiccatoi (spray, a letto fluidificato, ecc.) | ☑ | ☑ | ☑ | ☐ | ☐ | ☑ | ☐ | ☐ | ☑ | ☑ | ☑ |
| Essiccatoi a vassoio | ☑ | ☑ | ☑ | ☐ | ☐ | ☑ | ☐ | ☐ | ☐ | ☐ | ☑ |
| Trasporto pneumatico | ☑ | ☑ | ☑ | ☐ | ☐ | ☐ | ☐ | ☑ | ☑ | ☑ | ☐ |
| Coclee | ☑ | ☑ | ☑ | ☑ | ☐ | ☐ | ☐ | ☐ | ☑ | ☑ | ☐ |
| Trasferimento e caricamento silos, container, ecc. | ☑ | ☑ | ☑ | ☐ | ☐ | ☑ | ☐ | ☐ | ☑ | ☑ | ☐ |
| Impianti di depolverazione (elettrofiltri, tessuto, cicloni, ecc.) | ☑ | ☑ | ☑ | ☐ | ☐ | ☑ | ☐ | ☑ | ☑ | ☑ | ☐ |
Fonte: Ebadat, 2009
Nel caso le verifiche “brevi” sopra menzionate non siano soddisfatte allora dovremmo ipotizzare che la polvere combustibile possa essere esplosiva. I test dovranno essere quindi eseguiti in funzione del differente processo/apparecchio a cui faremo riferimento (Ebadat, 2009).
2.2 Le miscele ibride
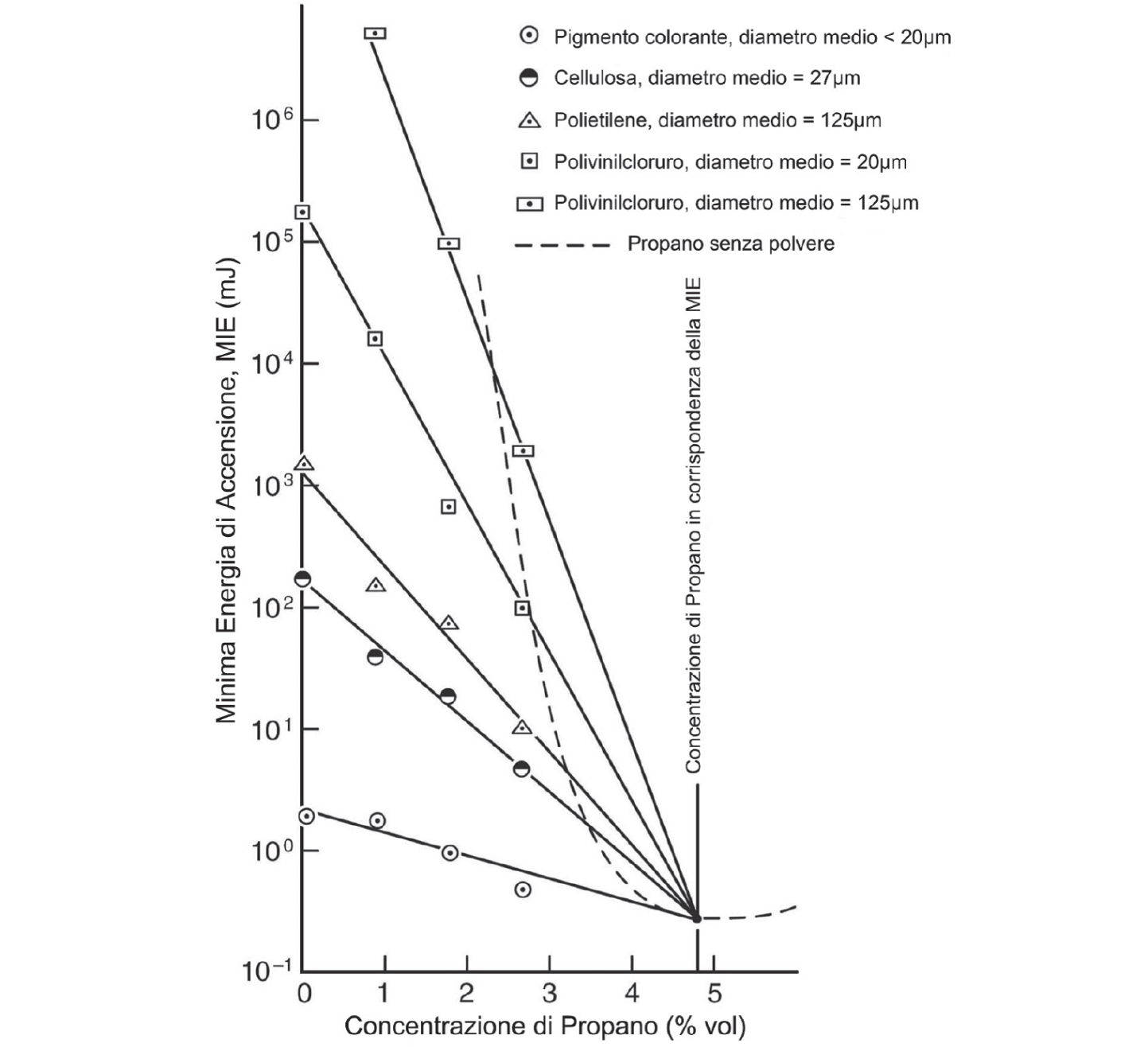
Per miscela ibrida si intende una miscela con l’aria di sostanze infiammabili in stati fisici diversi. Tipici sono gli esempi di miscele di polvere di coke con metano oppure di spray e vapori di benzina. La coesistenza di sostanze in stati fisici differenti modifica in modo significativo alcuni tra i parametri di esplosione descritti in precedenza. L’effetto maggiormente significativo è relativo alla rapida diminuzione della minima energia di accensione (MIE) delle polveri in presenza di gas o vapori infiammabili. Per esempio, la MIE di svariate polveri organiche in presenza di propano diminuisce molto rapidamente e si porta velocemente a valori corrispondenti alla MIE del propano a concentrazioni del 5%, diminuendo anche di svariati ordini di grandezza rispetto alla miscela polvere-aria originale. Tale effetto, evidente in coincidenza con il LEL del propano, risulta particolarmente evidente proprio in corrispondenza della concentrazione stechiometrica alla quale il gas infiammabile manifesta la più bassa energia di accensione (LMIE, Low MIE), come indica la Figura 2.13. Questa potente variazione della MIE causa un incremento del rischio di accensione soprattutto in presenza di scariche elettrostatiche non efficaci nell’innesco dell’ATEX dovuta alle sole polveri combustibili: il riferimento, in particolare, è alla cosiddetta scarica a spazzola (brush discharge), che descriveremo successivamente (Capitolo 6) che ha capacità di accendere ATEX-gas ma non ATEX-dust.
Anche i limiti di esplosione, in particolare il LEL, vengono influenzati nelle miscele ibride; è infatti possibile l’innesco di miscele ibride anche al di sotto del LEL di entrambe le sostanze miscelate. Questa variazione dovrà essere tenuta particolarmente in considerazione soprattutto durante i processi di essiccazione di polveri combustibili. La diminuzione del LEL delle miscele ibride segue la legge di Le Chatelier, tendendo a diminuire linearmente. Per esempio, il LEL della polvere di cellulosa miscelata a propano, che in condizioni normali si approssima al valore di circa 30 mg/m3, si azzera a concentrazioni di gas prossime al 2% (LEL del propano a condizioni atmosferiche). Infine, anche i parametri di esplosione necessari al dimensionamento dei sistemi di protezione contro le esplosioni risultano modificati nelle miscele ibride. In particolare la Norma UNI EN 14491 prevede che in presenza di miscele ibride con gas (o solvente) infiammabile assimilabile al propano si adottino, per polveri di classe St1 ed St2, i seguenti valori di progetto:
-
Pmax = 10 bar;
-
Kst = 500 bar·m/s.
La presenza di polveri St3 ibride richiede invece un approfondimento di analisi condotto da personale esperto dato che i sistemi di protezione standard non risulterebbero efficaci con parametri di esplosione così alterati.
Figura 2.13 – Variazione della MIE in miscele ibride polvere/propano (NFPA 68)
2.3 Le miscele infiammabili in atmosfere arricchite d’ossigeno
Il processo di combustione risulta notevolmente favorito se si arricchisce l’aria comburente con ossigeno21. Infatti nel caso di miscele gassose infiammabili, l’arricchimento di ossigeno induce un:
-
allargamento del campo di infiammabilità, soprattutto a causa dello spostamento dell’UEL come è rilevabile in Figura 2.1. Il LEL invece non viene particolarmente influenzato dall’aumento di concentrazione del gas ossidante. In Tabella 2.18 sono riportati alcuni esempi di estensione del campo di infiammabilità relativamente alle sostanze più comunemente presenti in ambito industriale;
-
aumento della velocità di combustione laminare. Di norma tale velocità aumenta di circa 10 volte rispetto alla velocità di combustione della miscela con aria atmosferica;
-
diminuzione estremamente marcata della minima energia di accensione. I gas infiammabili tendono a diminuire la MIE fino a 100 volte il valore comunemente ri-scontrabile in condizioni atmosferiche. Per esempio l’acetilene diminuisce la MIE da 0,017 mJ (aria) a 0,0002 mJ (ossigeno), il metano passa da 0,21 mJ (aria) a 0,003 mJ, l’etilene, infine, diminuisce la MIE da 0,07 mJ a 0,001 mJ;
-
la temperatura adiabatica di fiamma incrementa di circa 1000 °C;
-
la temperatura di accensione diminuisce di circa 10÷100 °C a seconda della sostanza e del metodo di prova utilizzato.
Analogamente si comportano i materiali solidi combustibili, soprattutto a causa della rilevante diminuzione della minima energia di accensione.
Alla luce di quanto indicato, in atmosfere arricchite d’ossigeno la classificazione delle sostanze infiammabili convenzionalmente utilizzata perde di significato, così come risultano inapplicabili le indicazioni progettuali per la costruzione di apparecchi elettrici e non elettrici ivi collocati, vista l’alterazione sostanziale di tutti gli aspetti afferenti alla sicurezza intrinseca delle energie in gioco nonché delle temperature di accensione.
2.4 Esempi applicativi ed approfondimenti
2.4.1 Ampliamento del campo di infiammabilità conseguente ad un aumento di pressione
Il campo di infiammabilità del metano a condizioni atmosferiche è compreso tra il 5% (LEL) e il 15% (UEL). Si vuole determinare di quanto incrementa il campo di esplosione a seguito di un aumento della pressione di 10 bar (relativi). Partendo dall’eq. 2.3 e considerando che la pressione assoluta di 10+1=11 bar è pari a 1,1 MPa, si ottiene:
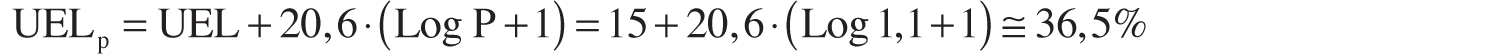
Dato che il LEL non viene particolarmente influenzato dalla pressione, l’incremento del campo di esplosione risulta pari a circa 21,5 punti percentuali (36,5%-15%=21,5%).
2.4.2 Calcolo del LOC dell’esano
Si vuole determinare il LOC dell’esano con il metodo proposto da Crowl e Louvar (Crowl et al., 2002).
La reazione di combustione dell’esano è la seguente:
Noto che sia il LEL dell’esano (1,2%), il calcolo del LOC è realizzato secondo la seguente logica:
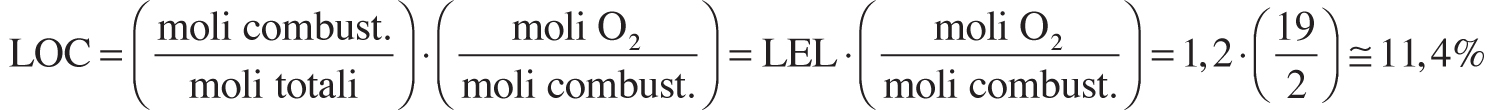
Il valore calcolato risulta compreso tra il LOC ottenibile con l’aggiunta di azoto (10%) ed il LOC ottenibile con l’inertizzazione ad anidride carbonica (12,5%) così come indicato in Tabella 2.18.
2.4.3 Le condizioni atmosferiche secondo la Direttiva 2014/34/UE
La Direttiva 214/34/UE è una direttiva di “nuovo approccio” e del “Nuovo Quadro Legislativo” che si propone di consentire la libera circolazione delle merci all’interno della UE. Ciò è possibile attraverso l’armonizzazione dei requisiti giuridici di sicurezza, seguendo un approccio basato sui rischi. Il suo obiettivo è anche eliminare, o quanto meno minimizzare, i rischi derivanti dall’uso di taluni prodotti all’interno o in relazione a un’atmosfera potenzialmente esplosiva. Il fabbricante deve fare delle ipotesi sull’impiego previsto del suo prodotto, incluso il contatto con atmosfere potenzialmente esplosive.
Una atmosfera esplosiva ai sensi della Direttiva 2014/34/UE è definita come una miscela:
-
di sostanze infiammabili allo stato di gas, vapori, nebbie o polveri;
-
con aria;
-
in determinate condizioni atmosferiche;
-
in cui, dopo l’innesco, la combustione si propaga all’insieme della miscela incombusta (occorre notare che – soprattutto in presenza di polvere – non sempre tutto il materiale combustibile viene consumato dalla combustione).
Un’atmosfera suscettibile di trasformarsi in atmosfera esplosiva a causa delle condizioni locali e/o operative viene definita atmosfera potenzialmente esplosiva. È solo a questo tipo di atmosfera potenzialmente esplosiva che sono destinati i prodotti oggetto della Direttiva 2014/34/UE.
È importante notare che i prodotti destinati ad essere utilizzati all’interno o in relazione a miscele che potrebbero rivelarsi potenzialmente esplosive non rientrano nella Direttiva 2014/34/UE qualora non siano presenti uno o più degli elementi caratteristici sopra elencati dal punto I) al punto IV).
Ad esempio:
-
Un prodotto all’interno di una miscela potenzialmente esplosiva senza la presenza di aria non rientra nel campo di applicazione della direttiva. Processi speciali di questo tipo necessitano di apparecchi progettati specificamente per tali rischi, in quanto gli apparecchi destinati ad essere utilizzati in atmosfere potenzialmente esplosive potrebbero provocare un rischio di innesco delle miscele in condizioni non atmosferiche.
-
Un apparecchio trasportatore in cui alcune parti, ma non tutte, si trovano sotto pressione atmosferica con pressioni interne diverse dalla pressione atmosferica, può rientrare nel campo di applicazione della Direttiva 2014/34/UE. Nell’effettuare una valutazione dei rischi risulterà evidente che, benché alcune parti dell’apparecchio descritto non rientrino nel campo di applicazione della Direttiva 2014/34/ UE durante il normale funzionamento (la pressione oscilla tra valori troppo bassi e troppo alti in relazione alle “condizioni atmosferiche”), alcune parti o spazi rientrano comunque nel campo di applicazione della medesima e l’apparecchio nel suo complesso vi rientra, almeno durante l’avviamento e l’arresto.
Entrambi gli esempi sotto riportati rientrano nel campo di applicazione della Direttiva 2014/34/UE:
-
una pompa a recupero dei vapori per una stazione di servizio è collegata in entrata e in uscita ad un’atmosfera potenzialmente esplosiva ai sensi della Direttiva 2014/34/ UE.
-
una pompa a vuoto che aspira da un contenitore sotto vuoto e convoglia la miscela in un recipiente a pressione o in una condotta a pressione. In questo caso, le parti interne della pompa non sono collegate ad un’atmosfera potenzialmente esplosiva ai sensi della Direttiva 2014/34/UE.
| ⇒ | Nota: il fabbricante può anche voler vendere questo apparecchio per un impiego in
condizioni atmosferiche all’ingresso e all’uscita, in tal caso si applicherà il caso
a). In ogni caso, deve essere considerato l’intero ciclo di lavoro, incluso l’avviamento e l’arresto, che potrebbe dar vita ad una pressione atmosferica. Se l’apparecchio non è destinato all’impiego in condizioni atmosferiche, la direttiva non si applica. Deve essere effettuata la valutazione dei rischi in base alla Direttiva 99/92/CE. Se l’utente non è in grado di garantire l’assenza di un’atmosfera potenzialmente esplosiva, l’avviamento e l’arresto sono rilevanti per stabilire l’applicazione della direttiva. |
2.4.4 Calcolo della MIE dell’ATEX della polvere di latte disidratato a 100 °C
La MIE a temperatura ambiente di un campione di latte in polvere testato dal BIA tedesco risulta pari a 75 mJ (Tabella 2.19). Si vuole valutare il decremento della MIE di tale sostanza portato a 100 °C. Applicando l’eq. 2.7 si ottiene:
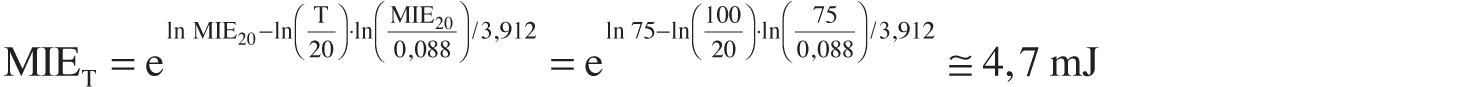
Il modello indica una drastica riduzione della MIE della polvere surriscaldata. Un incremento di circa 80 °C determina una riduzione della MIE da 75 mJ a circa 5 mJ. Tale dato risulta coerente con quanto indicato da Barton (Barton, 2002)22.
2.4.5 Calcolo delle temperature limite per uno stoccaggio di acetone
Si vuole procedere alla verifica del livello di saturazione dei vapori all’interno di serbatoi metallici fuori terra contenenti acetone. A tal fine si calcolano le temperature limite inferiore (TLI) e superiore (TLS) e si confronteranno con il Flash Point della sostanza e la temperatura ambiente nel quale i serbatoi verranno collocati.
Si procede alla verifica della TLI attraverso l’eq. 2.9 assumendo le costanti di Antoine (cfr. Allegato B) ed il LEL per l’acetone (Tabella 2.18) si ha, quindi:
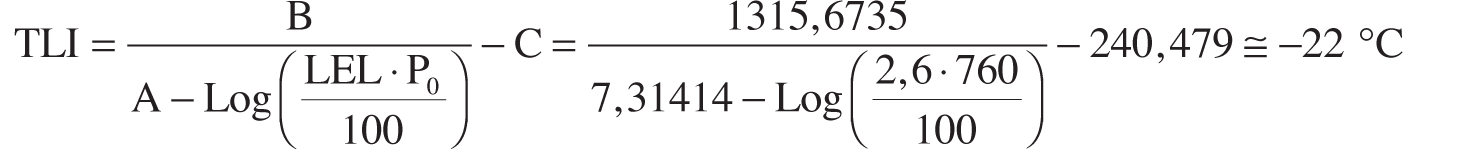
Tale valore risulta poco inferiore al punto di infiammabilità dell’acetone (–17 °C). Il TLS è invece calcolato grazie all’eq. 2.10.
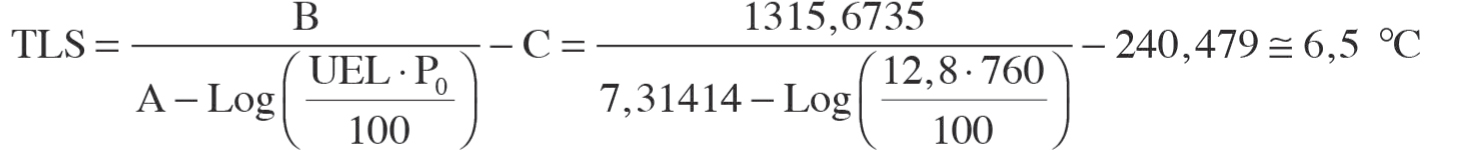
Il TLS risulta superiore alle temperature ambientali invernali; non è pertanto possibile escludere la presenza di ATEX all’interno del tank fuori terra contando esclusivamente sulla saturazione ed il recupero dei vapori infiammabili.
L’applicazione della procedura illustrata alle miscele complesse non è stata provata estesamente.
2.4.6 Calcolo della modifica del punto di infiammabilità in una miscela metanolo-acqua
Si vuole calcolare il punto di infiammabilità di una miscela contenente (in massa) il 75% di metanolo ed il 25% di acqua. Il metanolo è perfettamente miscibile in acqua ed il sistema metanolo-acqua non è azeotropico. Il metanolo puro possiede il seguente punto di infiammabilità (Tabella 2.18):
FP = 10 °C
La tensione di vapore corrispondente si calcola con l’equazione di Antoine (cfr. Allegato B):
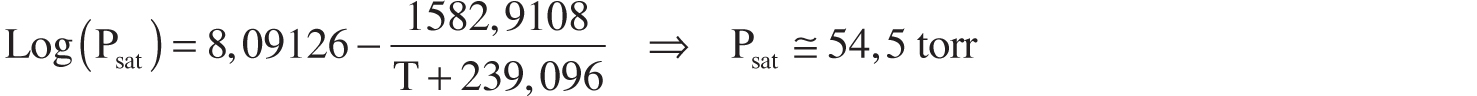
Ipotizzando una miscela 25% acqua e 75% acetone (in massa) si ottengono rispettivamente 1,39 moli d’acqua e 2,34 moli di acetone. La frazione molare del metanolo è dunque pari a x = 0,63 (Tabella 2.16).
Tabella 2.16 – Calcolo della frazione molare del metanolo
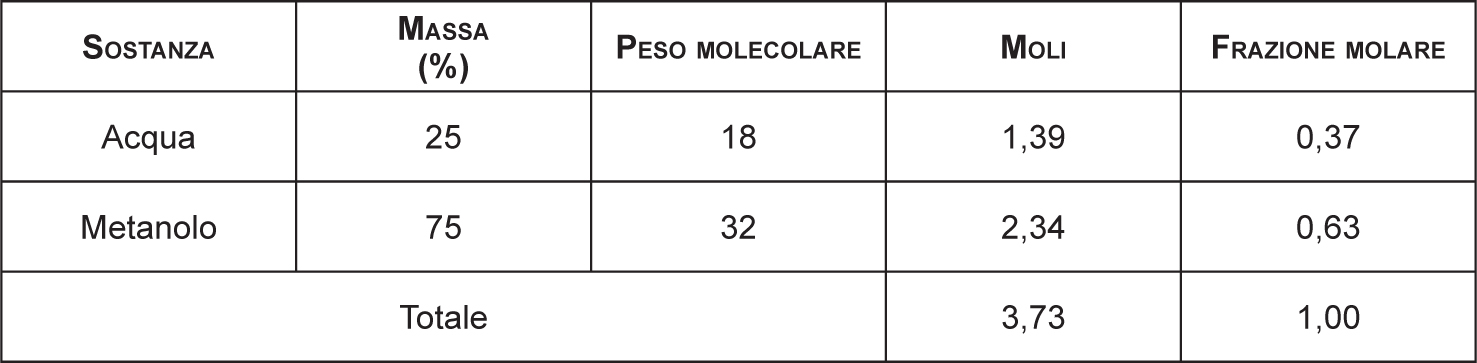
La pressione di vapore in corrispondenza di questa frazione molare è pari a:

Avendo applicato la legge di Raoult.
La temperatura di Flash Point per la miscela è quindi pari a:
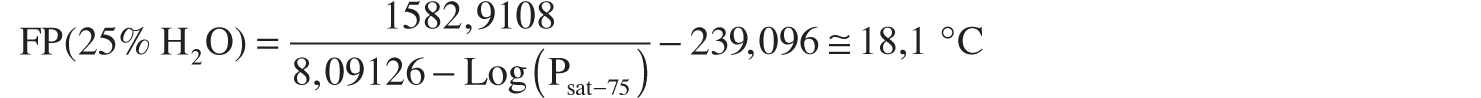
Comunque inferiore alla temperatura ambiente stimata (20 °C). La miscela rimane pertanto infiammabile alla temperatura ambiente. L’applicazione della procedura illustrata alle miscele complesse non è stata provata estesamente. Da un punto pratico la determinazione sperimentale del punto di infiammabilità dei preparati risulta sempre consigliabile.
2.4.7 Caratterizzazione statistica di un campionamento di polveri
Un’azienda operante nel settore della lavorazione di metalli leggeri ha necessità di procedere ad un intervento di protezione da eseguirsi sull’impianto di filtraggio posto a valle delle lavorazioni di stabilimento. All’interno del filtro durante l’esercizio giungono polveri di alluminio provenienti dalle varie e diverse lavorazioni che si eseguono nei reparti e di cui è difficoltoso tracciare profilo granulometrico di sintesi. Al fine di procedere ad una corretta valutazione dei parametri di esplosione (Kst, Pmax), si decide di ricorrere ad una preliminare valutazione granulometrica delle polveri presenti nel filtro. Tale valutazione sarà finalizzata a determinare i margini di variabilità del diametro medio delle polveri trattate. Il test di esplosione sarà successivamente realizzato su polveri che siano rappresentative del processo in essere presso l’azienda.
Il piano di prelievo, deciso in accordo con i responsabili di ingegneria, produzione e manutenzione, prevede quindi l’estrazione, nel corso di una settimana (in cinque giorni successivi e ad orari stabiliti), di cinque campioni di polveri dal filtro oggetto di analisi provenienti dalla zona delle maniche di filtraggio. Tale modo di procedere viene ritenuto sufficientemente rappresentativo del complessivo delle lavorazioni che vengono effettuate.
I risultati dell’analisi del diametro medio delle polveri (dmi) è il seguente: 75 µm, 90 µm, 65 µm, 80 µm, 90 µm. La media campionaria è quindi pari a:

dove n è stato assunto pari a 5.
Lo scarto quadratico medio della distribuzione risulta pari a:

Utilizzando pertanto la distribuzione t-Student con 4 gradi di libertà (n-1=4) e assumendo un intervallo di confidenza del 95%, si ottiene un valore di t0,975 pari a 2,78, in corrispondenza del quale il 2,5% dell’area è compreso in ciascuna coda della distribuzione t (cfr. Allegato C). L’intervallo che conterrà il 95% dei diametri medi del processo sarà quindi il seguente:
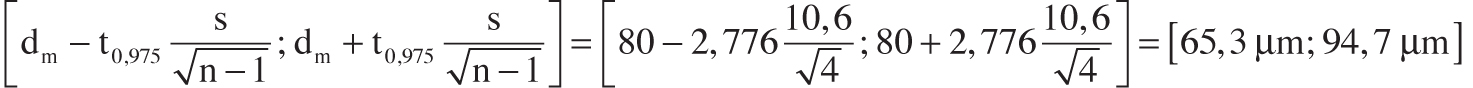
Il processo di produzione genererà pertanto polveri che nel 95% dei casi possiederanno diametro medio compreso tra 65,3 µm e 94,7 µm. Il campione di polveri sul quale effettuare i test dovrà pertanto essere selezionato con diametro medio il più possibile prossimo al valore minimo del campo di variabilità. Si considereranno accettabili e rappresentativi delle polveri del processo, tutti i campioni estratti che possiederanno un diametro medio inferiore a:
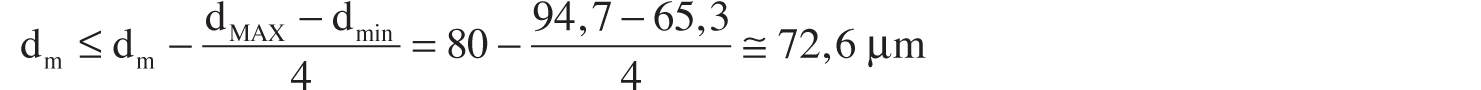
2.4.8 Calcolo del valore di Kg dell’acetone
Si vuole procedere alla determinazione approssimata del valore Kg dell’acetone, sostanza non tabellata in NFPA 68. La sostanza di confronto scelta è l’etano. Adottando i valori velocità di combustione laminare e del Kg (quest’ultimo del solo etano) e successivamente applicando l’eq. 2.13, si ottiene (Tabella 2.18):
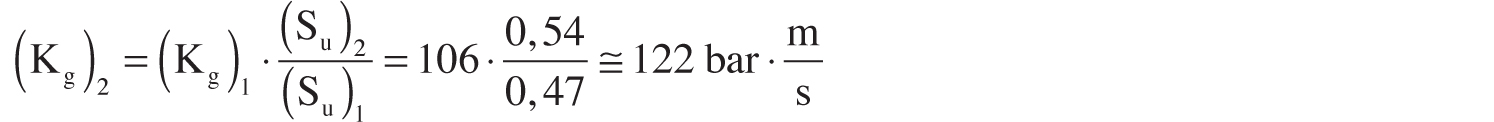
Tale valore, in caso di progettazione di misure di protezione, deve essere comunque validato con test di esplosione specifici.
2.4.9 Approfondimento: Proprietà particolari di alcuni gas e vapori infiammabili
Alcune sostanze infiammabili se sottoposte ai test precedentemente indicati manifestano, sotto certe condizioni di prova, proprietà impreviste o inaspettate. Nel seguito si vuole fornire un elenco sicuramente non esaustivo della problematica.
2.4.9.1 Acetilene
L’acetilene è un gas che possiede un’entalpia di formazione positiva e che può decomporsi in modo esplosivo anche in assenza di aria. L’acetilene può reagire esplosivamente a pressione atmosferica in tubazioni di trasporto di ampio diametro. Sono inoltre noti numerosi incidenti a generatori di acetilene quando un guasto ai sistemi di riduzione della pressione a consentito di raggiungere pressioni pari a circa 1,4 bar in presenza di umidità.
2.4.9.2 Etilene
L’etilene è un gas che possiede un’entalpia di formazione positiva e che può decomporsi in modo esplosivo anche in assenza di aria. L’etilene può reagire esplosivamente ad alte pressioni.
2.4.9.3 Gas di cokeria
Il gas di cokeria è una miscela di idrogeno, monossido di carbonio e metano. Se la somma della concentrazione di idrogeno e monossido di carbonio risulta inferiore al 75% del totale il gas è classificabile di gruppo IIB. Nel caso tale ipotesi non sia verificata, il gas è complessivamente classificato di gruppo IIC.
2.4.9.4 Idrazina
I vapori di idrazina, una volta accesi, sviluppano una reazione di decomposizione esotermica anche in assenza di aria o di altri ossidanti. L’idrazina possiede una temperatura di accensione variabile in funzione della superficie con la quale risulta in contatto. Per esempio, in aria, essa manifesta una temperatura di autoaccensione pari a 23 °C a contatto con la ruggine, 156 °C a contatto con l’acciaio inossidabile mentre a contatto con il vetro si accende a 270 °C.
2.4.9.5 Metano industriale
Il metano industriale, come il gas naturale, è classificato di gruppo IIA a condizione che non contenga più del 15% di idrogeno. Una miscela di metano con altre sostanze di gruppo IIA (in qualsiasi proporzione) è classificato comunque di gruppo IIA.
2.4.10 Confronto tra l’ATEX dovuta a gas naturale e a GPL
Il gas naturale (GN) ed il gas di petrolio liquefatto (GPL) sono nostri compagni quotidiani, sia negli ambienti domestici così come sul lavoro. Essi spesse volte sono assimilati in termini di rischio poiché, nella maggior parte dei casi, vengono utilizzati per scopi analoghi (riscaldamento, cottura cibi, ecc.). Non è però sempre così, dato che le due miscele possiedono sia origini tecnologiche differenti sia utilizzi ulteriori rispetto alla loro semplice combustione.
Ci si propone, con questo approfondimento, di differenziarli in termini di rischio di esplosione e, per fare questo, vista la variabilità della loro composizione, utilizzerò i parametri di infiammabilità ed esplosione dei loro costituenti principali:
-
il metano (CH4) per il GN;
-
il propano (C3H8) per il GPL.
2.4.10.1 Parametri chimico-fisici
L’indicatore che maggiormente caratterizza i due gas da un punto di vista dell’applicazione è il potere calorifico inferiore (PCI). Metano e propano possiedono, in questo senso, caratteristiche analoghe poiché i PCI/kg risultano sostanzialmente assimilabili:
-
PCICH4 = 50,0 MJ/kg;
-
PCIC3H8 = 46,35 MJ/kg.
Ciò che li differenzia sono le modalità di stoccaggio. La capacità volumetrica di trasporto di energia risulta, in questo senso, modificata rispetto al parametro riferito alla massa.
Il GN viene prevalentemente trasmesso via “tubo” e ridotto grazie ad una serie di stadi ad alta, media e bassa pressione oppure, nel caso per esempio dell’autotrazione o di particolari lavorazioni industriali, stoccato sotto forma di gas naturale compresso (GNC). GNC che riesce a immagazzinare, per ogni litro, l’equivalente di circa 9 MJ (cioè 9 GJ/m3 ≌ 240 barg).
La miscela propano/butano tipica del gas liquefatto GPL contiene invece, con pressioni di stoccaggio molto più limitate (circa 7 barg), un’energia di circa 25 GJ/m3 mentre il gas naturale liquefatto, GNL23, ottenuto per sottoraffreddamento del GN, arriva a 22 GJ/m3.
Per avere un termine di confronto, il gasolio possiede una densità energetica per volume di circa 34-35 GJ/m3. Riepilogando, quindi:
-
GNC: 9 GJ/m3 ≌ 240 barg;
-
GNL: 22 GJ/m3;
-
GPL: 25 GJ/m3.
Si consideri che la tecnologia di liquefazione per pressione del GPL permette una riduzione di circa 260 volte della densità dei vapori (rispetto ad iniziali condizioni atmosferiche) mentre con il GNC l’aumento di tale parametro sarà dipendente linearmente dal livello di compressione rispetto all’ambiente (200-240 barg)24. Infine il GNL aumenta di circa 600 volte la densità, sempre rispetto alle condizioni atmosferiche.
A questo si aggiunga che la tipologia di rilascio da un contenimento di GNC risulterà indipendente dalla posizione della sorgente di emissione sulla membratura di contenimento (si genererà sempre un rilascio a getto supersonico di gas infiammabile ad alta pressione) mentre sia nel caso di GPL come nel caso del GNL lo scenario incidentale dipenderà da tale collocazione in relazione al battente di liquido. In particolare, nel caso del GPL, se la perdita di contenimento avesse origine al di sopra del battente liquido, si concretizzerebbe un’emissione di vapori mentre se, per converso, tale guasto avesse luogo al di sotto si creerebbe un rilascio di liquido in ebollizione (flashing) con formazione di pozza al suolo (rainout) che risulterebbe, peraltro, molto più stabile nel caso del GNL rispetto al GPL. La liquefazione per sottoraffreddamento, infatti, consente condizioni di equilibrio termodinamico maggiori rispetto alla liquefazione per pressione. Non nascondiamo che molte altre sono le conseguenze di un rilascio di gas liquefatto che, purtroppo per ragioni di spazio, si tralasciano.
Figura 2.14 – Scenari di rilascio di GPL (Boot, 2015)
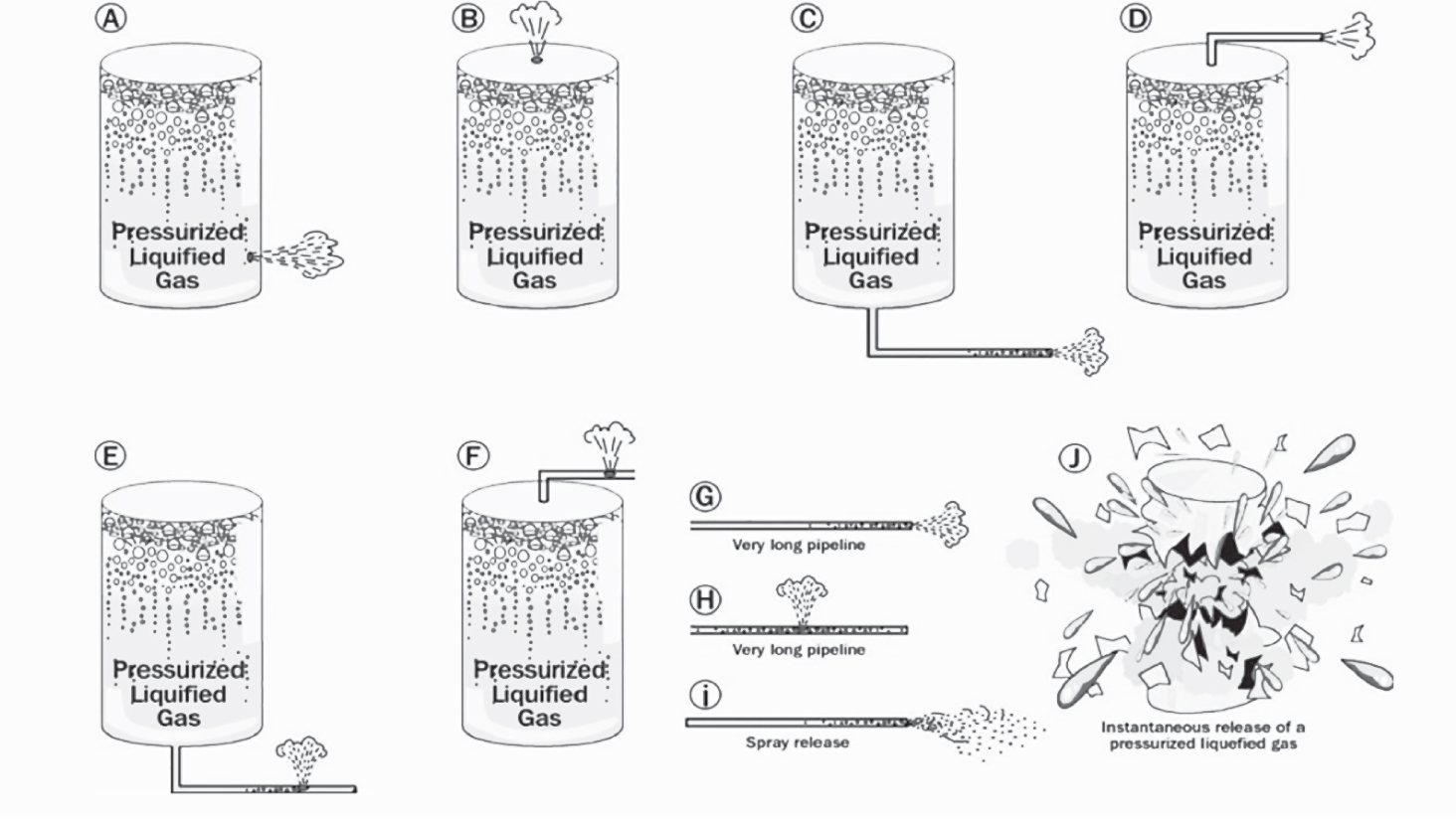
Nel caso in cui il guasto di tenuta abbia luogo nelle tubazioni di trasporto, per esempio, le dinamiche di rilascio e dispersione si articolano ulteriormente (cfr. scenari A-I, Figura 2.14).
2.4.10.2 Parametri di combustione/esplosione
Le velocità di combustione laminare delle due sostanze indagate risultano molto simili, con una leggera maggior velocità del propano che non conduce, di per sé, a particolari aggravi di pericolosità. Si ha:
-
vcl,CH4 = 40 cm/s;
-
vcl,C3H8 = 46 cm/s.
Nemmeno nel caso della pressione massima di esplosione esistono differenze significative. Il propano, avendo una temperatura adiabatica di fiamma lievemente superiore a quella del metano, genera, nel test di esplosione in sfera di Siwek, una maggior sovrappressione:
-
Pmax,CH4 = 7,1 barg;
-
Pmax,C3H8 = 7,9 barg.
La prima sorpresa in termini di parametri di esplosione è evidenziata dalla costante specifica di esplosione, Kg25, rappresentativa della velocità di incremento della pressione. Il propano possiede una velocità di incremento pressorio doppia rispetto al metano.
La violenza attesa dell’esplosione è quindi molto maggiore nel caso del GPL in paragone al GN:
-
Kg,CH4 = 55 bar m/s;
-
Kg,C3H8 = 100 bar m/s.
Tale fatto viene tenuto in considerazione in un particolare (e sofisticato) metodo di simulazione degli effetti dell’esplosione in ambiente non confinato (UVCE) denominato Baker-Strehlow-Tang. Questa metodologia di valutazione include il metano nella classe bassa di reattività (la III) mentre il propano è ricompreso in classe II (moderata reattività). La classe I (alta reattività) è riservata ai soli acetilene, ossido di etilene ed idrogeno.
Il maggior Kg del propano configura, inevitabilmente, la necessità, in caso di sfogo dell’esplosione, di superfici di minima resistenza di ampiezza maggiore rispetto al gas naturale. Oppure, viceversa, a parità di area delle superfici di sfogo (es. finestrature in un locale chiuso), il propano determinerà una pressione di esplosione ridotta (Pred,max) molto maggiore rispetto a quella prodotta dal gas naturale.
Figura 2.15 – Dinamica di esplosione di gas naturale all’interno di un’abitazione (Harris, 1983)

Si tenga inoltre in considerazione il fatto che l’esplosione di GPL originata in un locale chiuso troverà maggiori difficoltà allo sfogo rispetto alla deflagrazione di gas naturale (che avrà luogo, verosimilmente, affacciata alle vetrature). La maggior “maturazione” dell’esplosione all’interno del locale sarà, in questo senso, un fattore aggravante, in termini di danno causato, nel GPL rispetto al gas naturale.
Figura 2.16 – Dinamica di esplosione di GPL all’interno di un’abitazione (Harris, 1983)

Inoltre, a fronte di energie di accensione tra loro paragonabili (sia metano che propano sono sostanze di gruppo IIA), si rileva una estensione del campo di esplosione del metano, rispetto al propano, di almeno quattro punti percentuali.
-
LFL,UFLCH4 = 4,4-17% (vol);
-
LFL,UFLC3H8 = 1,7-10,9% (vol).
Questo fatto ha conseguenze dirette nell’ambito della classificazione delle zone a rischio di esplosione; la combinazione tra gli effetti della massa molare (molto maggiore nel propano rispetto al metano) e del LFL (meno della metà nel propano rispetto al metano) provoca, infatti, un’ampiezza di zona pericolosa, nel campo vicino, simile (con il metano, a parità di variabili di emissione, si calcolano distanze pericolose pari ai 3/4 di quelle del propano).
Le ampiezze delle zone di classificazione risultano invece fortemente modificate dalle Norme CEI EN 60079-10-1:2016 e EN IEC 60079-10-1:2021 le quali includono nel calcolo della zona di classificazione anche la tipologia di gas (heavy, diffusive e jet gas).
In presenza di gas pesanti, come è il caso del GPL, le distanze di classificazione aumentano di un ordine di grandezza rispetto ai jet di gas infiammabili leggeri (del quale il metano fa parte). Il GPL, a differenza del gas naturale, tende infatti ad avere un comportamento “passivo” rispetto al GN il quale, avendo una densità (circa) dimezzata rispetto a quella dell’aria tenderà a “galleggiare” per principio di Archimede. In altri termini se diamo al gas naturale la possibilità di “fuggire”, questo lo farà con molta efficacia. Il GPL è invece un gas “pigro” che staziona in prossimità del luogo di rilascio e si sposta prevalentemente in conseguenza dei soli spostamenti locali dell’aria (attenzione però alla presenza di cavedi, tombini, ecc.).
2.4.10.3 Conclusioni
Alla luce delle considerazioni esposte (alcune, per la verità, appena accennate altre nemmeno affrontate26) possiamo trarre le seguenti conclusioni:
-
gli stoccaggi di GPL possono essere coinvolti in gravissimi incidenti industriali (BLEVE, flashing, rainout). A tali scenari incidentali non sono invece vulnerabili i depositi di CNG;
-
le esplosioni di nubi di vapori (UVCE) che coinvolgono GPL evidenziano capacità distruttive molto maggiori rispetto a quelle del gas naturale;
-
i rilasci di gas liquefatti (GPL, GNL) generano nubi dense e passive mentre il GN, anche se derivante da stoccaggi in forma compressa, tende a “muoversi autonomamente”27 pur in assenza di rilevante ventilazione generale28;
-
lo studio della ventilazione degli ambienti chiusi risulta di straordinaria importanza e non può limitarsi al solo calcolo della portata minima di ventilazione, come già ci ha insegnato Harris 35 anni fa. La collocazione ed il “lavaggio” dei locali deve essere assicurato, a parità di portata di ventilazione, grazie ad un corretto posizionamento delle aperture.
2.4.11 Le polveri marginalmente esplosive
Nel corso degli ultimi anni si sta facendo strada un’ipotesi molto particolare: una parte delle polveri combustibili, che noi consideriamo esplosive a fini ATEX, in realtà pare lo siano solo “marginalmente”.
Per spiegare meglio l’affermazione precedente è necessario preliminarmente chiarire che i test di esplosione realizzati conformemente agli standard EN 14034-X prevedono l’utilizzo di un reattore di prova avente un volume pari a 1 m3.
Il problema, da sempre presente in un simile impianto, è che richiede una notevole quantità di polvere per la realizzazione del test (teniamo peraltro presente che, per motivi di affidabilità statistica, i laboratori eseguono più volte il test di esplosione prima di fornire i parametri caratteristici della polvere).
Se da un lato, quindi, le polveri provenienti da materiali di scarto inducono pochi oneri economici per il loro reperimento in quantità rilevante, dall’altro ci possono essere polveri da testare, costituite da materia prima, che possiedono un costo a volte non indifferente. In quest’ultimo caso chi volesse eseguire il test di esplosione dovrebbe sostenere, oltre agli oneri diretti del laboratorio, anche i costi relativi al valore connesso alla perdita di materia prima. E, se discutiamo di prodotti farmaceutici, per esempio, il parametro economico per l’esecuzione di un semplice test di esplosione, in un dispositivo da 1 m3, potrebbe diventare un ostacolo insormontabile. Ecco perché, in ambito scientifico (prima) e normativo (dopo) si è fatta strada l’ipotesi di utilizzare volumi più ridotti per l’esecuzione di queste prove di esplosione. Bartknecht, nel 1989, dimostra (per un ristretto numero di polveri), l’equivalenza tra i risultati ottenuti in volume di test da 1 m3 rispetto a quelli ottenibili con sfere di test di 20 litri di capacità. La relazione cubica mantiene la propria validità anche in tale, minima, configurazione volumetrica.
Tale equivalenza, dimostrata parzialmente dal Bartknecht, viene fatta propria dalla Norma tecnica, già citata in precedenza, la quale, nell’allegato C, specifica che “An alternative type of test equipment, for which conformity has been proven, is the 20 l sphere”.
La soluzione è quindi trovata: si sostituisce la sfera da 1 m3 (1000 litri) con un volume 50 volte inferiore.
La massa delle polveri necessarie all’esecuzione dei test si riducono drasticamente e il problema del costo di esecuzione degli stessi, connesso alla perdita di materia prima, si demoltiplica in proporzione.
Teniamo in considerazione che il test nella sfera da 20 litri viene realizzato in presenza di una pressione di dispersione della polvere pari a 20 bar e con energie di innesco uguali a 10 kJ.
Condizioni estreme, evidentemente non riscontrabili nella maggioranza delle situazioni industriali reali. Condizioni, peraltro, in grado di “far esplodere” molte polveri che, in contesti ordinari probabilmente avrebbero manifestato, al più, un problema di semplice prevenzione incendi.
A questa considerazione si aggiungono i test eseguiti dall’INERIS francese (Proust, 2007) su polveri combustibili (non metalliche) i quali evidenziano, al di là delle differenze nei parametri in uscita tra i due apparecchi di prova (Kst e Pmax)29, che alcune polveri combustibili esplodono in sfera da 20 litri ma non esplodono nel classico test da 1 m3. Si discute, in particolare, di polveri combustibili con Kst (misurato in sfera da 20 litri) inferiore a 45-50 bar·m/s.
Il problema non è irrilevante, quindi. È possibile che ci siano situazioni nelle quali il problema ATEX sia sopravvalutato a causa di test di esplosione eseguiti con un vantaggio di sicurezza forse troppo elevato (cfr. Tabella 2.17).
Tabella 2.17 – Parametri di esplosione determinati in sfera da 1 m3 e da 20 litri (Proust et al. 2007)
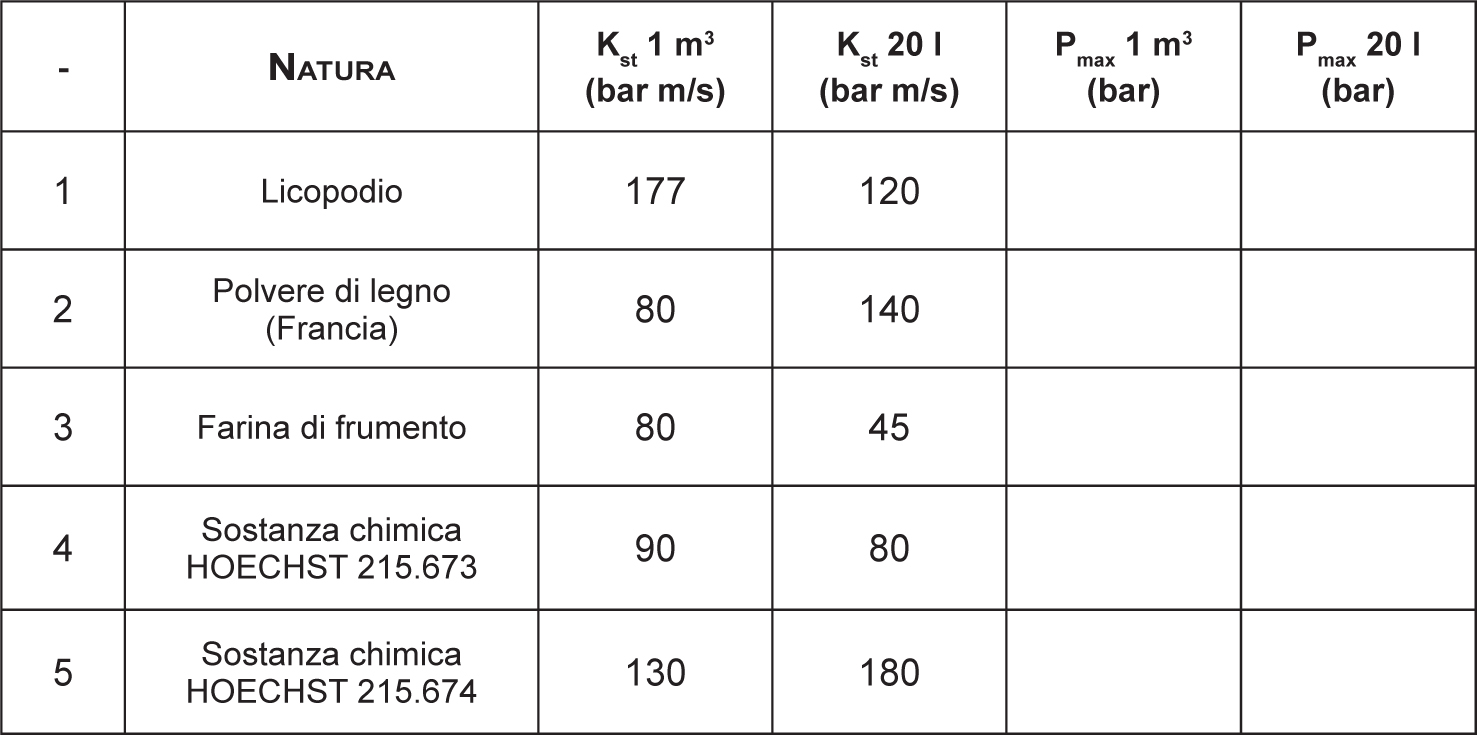
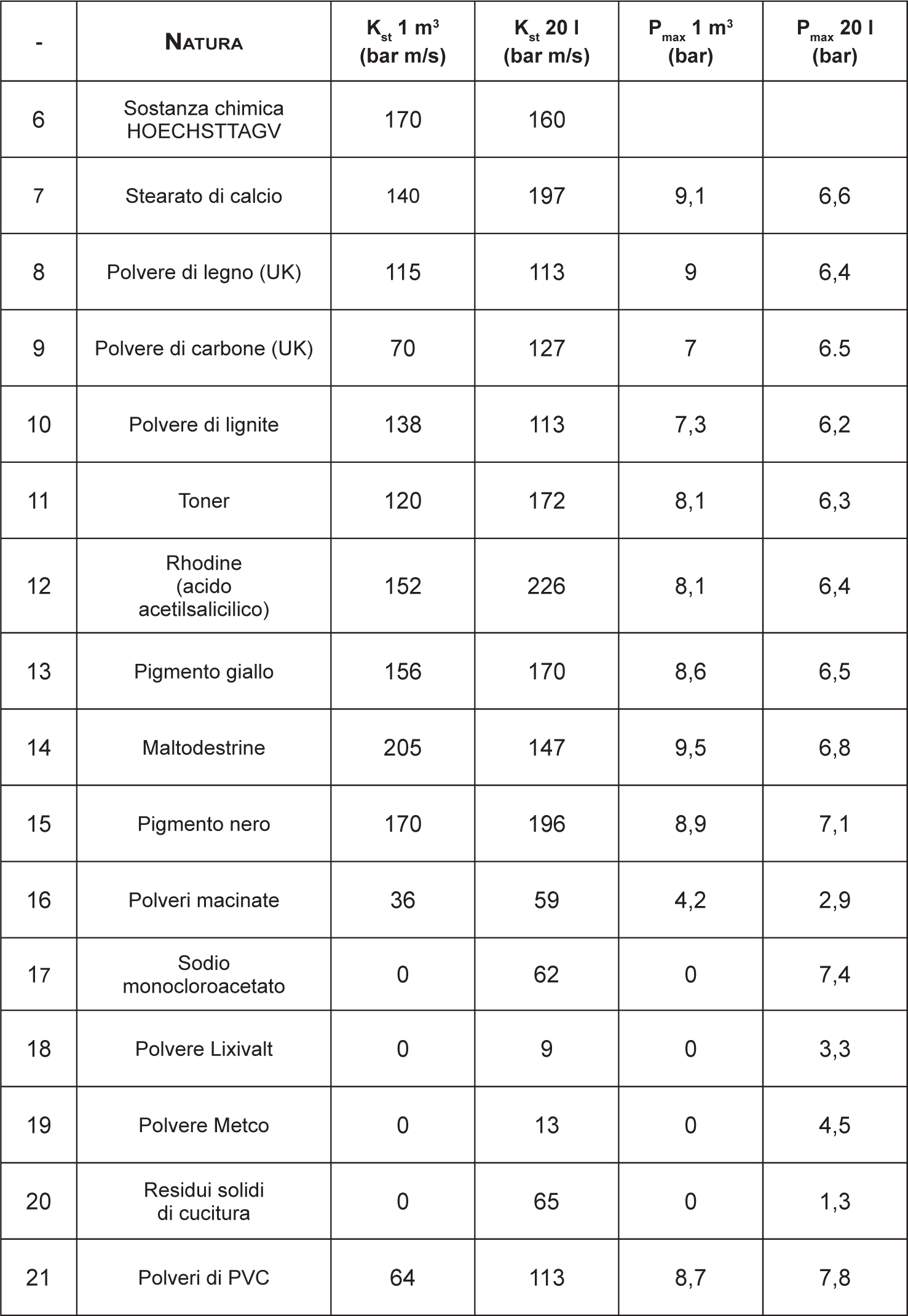
Peraltro di tale anomalia ne fa menzione pure la Norma NFPA 654:2013 che specifica quanto segue: “(…) There is some possibility that a sample will result in a false positive in the 20 L sphere when tested by the ASTM E 1226 screening test or the ASTM E 1515 test. This is due to the high energy ignition source overdriving the test. When the lowest ignition energy allowed by either method still results in a positive result, the owner/operator can elect to determine whether the sample is a combustible dust with screening tests performed in a larger scale (≥1 m3) enclosure, which is less susceptible to overdriving and thus will provide more realistic results (…)”.
Il fenomeno definito di overdriving può causare quindi, a detta di NFPA 654, la generazione di falsi positivi. Tali polveri, con Kst dell’ordine di 45-50 bar·m/s, vengono definite da Amyotte “marginalmente esplosive”.
Purtroppo, però, la situazione è ancora più complicata di quanto finora illustrato. Esistono infatti dati sperimentali che dimostrano come il comportamento “marginalmente esplosivo” non si evidenzi con le polveri di metalli che, al contrario delle polveri organiche, manifestano, anche per limitati valori di Kst, parametri più gravosi nel test in 1 m3 rispetto a quello in sfera da 20 litri.
La conclusione che quindi possiamo trarre da queste nuove ricerche è la seguente:
-
le polveri organiche aventi Kst dell’ordine di 45-50 bar·m/s potrebbero non essere realmente esplosive nelle normali condizioni di impiego;
-
le polveri metalliche con Kst molto bassi potrebbero manifestare violenze di esplosione maggiori rispetto a quelle misurate in laboratorio con sfera da 20 litri.
Peraltro, se teniamo pure in considerazione il fatto che le polveri “marginalmente esplosive” rappresentano un corposo sottoinsieme delle polveri di classe St1 le quali, a loro volta, sono il gruppo maggiormente rappresentativo nel panorama manifatturiero, bene si comprende l’impatto sia impiantistico sia economico che tale presunta sopravvalutazione potrebbe aver determinato nel corso di questi ultimi 20 anni.
2.4.12 Variabilità delle caratteristiche di esplosione nelle polveri combustibili
Con questo approfondimento si vuole presentare una raccolta empirica di evidenze inerente la variabilità dei parametri di esplosione delle polveri combustibili. Tali parametri rappresentano, infatti, un tema sensibile poiché da essi dipendono le specifiche misure di prevenzione e protezione ATEX. Ci concentreremo sulle variazioni di alcuni parametri significativi (MIE, MEC, Pmax/Pex, Kst e (dp/dt)ex) al variare del diametro medio del particolato e dell’umidità in esso contenuta.
Correliamo, innanzi tutti, la minima energia di accensione e l’LFL/MEC delle polveri di lattosio riepilogate nel BIA Report 13/1997 (vedi Figura 2.17). Ad un aumento del diametro medio si nota una limitata (e non molto affidabile, R2 = 0,31) correlazione positiva tra LFL/MEC. Tende ad aumentare di poco, cioè, la minima concentrazione esplosiva all’aumentare del diametro medio della polvere.
Se invece osserviamo l’andamento della MIE questa, nel passaggio da 25 e 225 µm, aumenta di due ordini di grandezza: si passa, cioè, da una polvere ad altissimo rischio di innesco vulnerabile a scariche elettrostatiche di tipo “brush” (aventi energia massima di 4 mJ) a polveri definibili Hard To Ignite (HTI) con MIE > 1000 mJ.
L’andamento della MIE, cioè, è correlabile ad una funzione dm3.
Nel caso delle nanopolveri tale correlazione è invece stimata proporzionale a dm0,5.
Figura 2.17 – MIE & LFL/MEC vs. dm [Polveri di lattosio]
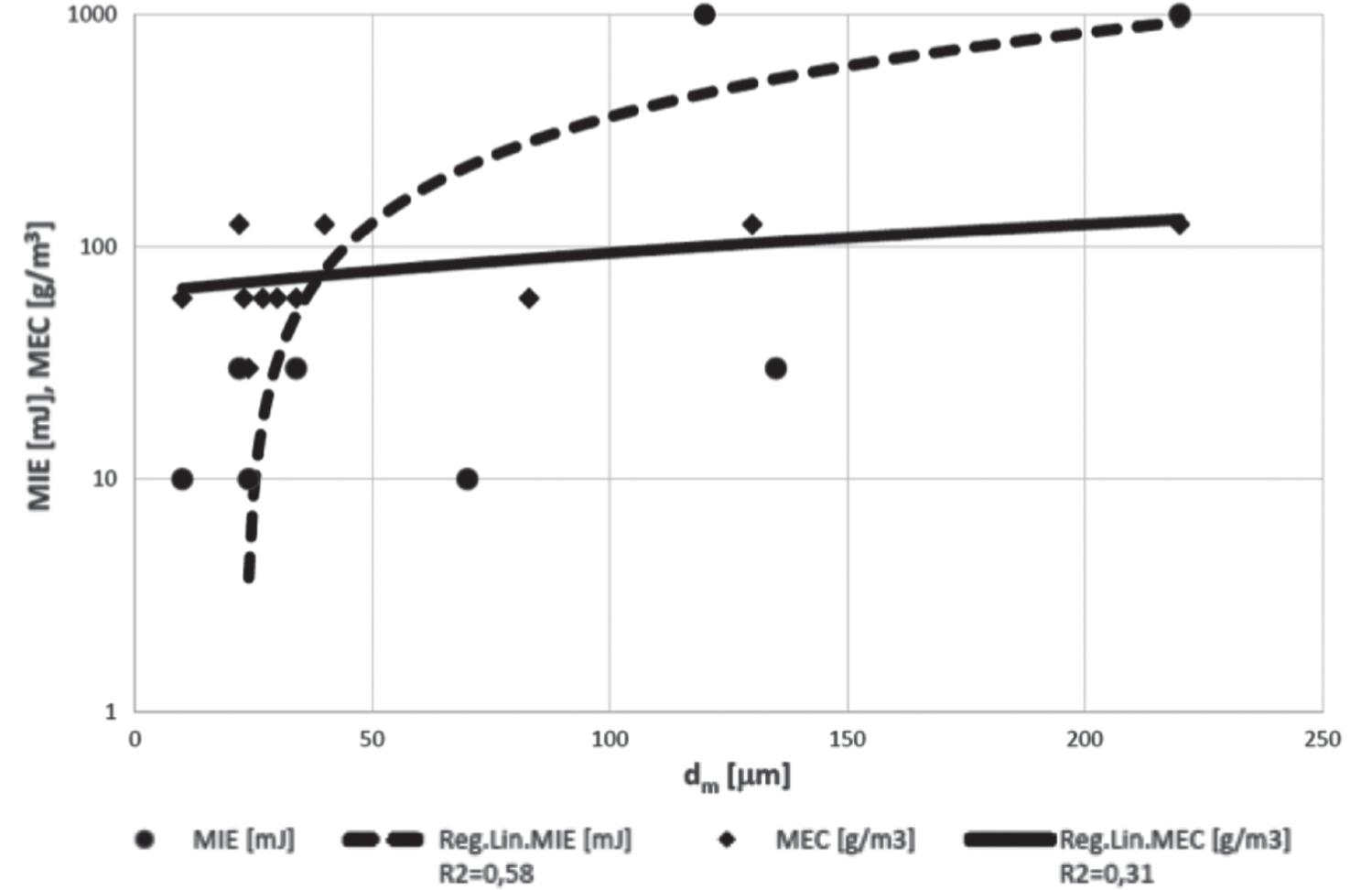
Fonte: BIA Report 13/1997
Il caso delle polveri di zucchero (vedi Figura 2.18) differisce rispetto alle polveri di lattosio appena illustrate. L’LFL/MEC tende infatti ad aumentare con maggior evidenza all’aumentare della granulometria (le polveri fini si assestano su LFL/MEC pari a 60 g/m3 mentre con diametri superiori a 250 µm si correlano a MEC compresi tra 500 e 750 g/m3). Valori, questi ultimi, davvero molto elevati. L’aumento del diametro medio granulometrico è correlato, altresì, ad un radicale abbassamento del Kst (un ordine di grandezza tra i 25 e i 300 µm) a fronte di una diminuzione molto più contenuta della massima pressione di esplosione (Pmax).
Spostiamoci ora allo studio delle variazioni della MIE in presenza di umidità (vedi Figura 2.19) oppure di polveri inerti, miscelati alle polveri combustibili, utilizzando studi che hanno approfondito il comportamento del toner per stampanti (polvere di carbonio). La prima considerazione è che non tutte le sostanze inerti miscelate alle polveri combustibili hanno medesima efficacia. Il bicarbonato di sodio (NaHCO3), una tipica polvere per estintori, non ha alcun effetto sulle caratteristiche di innesco del carbonio. Per converso, il carbonato di calcio (CaCO3) manifesta efficacia a partire da concentrazioni superiori al 50% rendendo la polvere di carbone difficile da accendere (HTI) a concentrazioni superiori al 70% (wt/wt). A quest’ultimo riguardo, per il carbone bituminoso viene identificato un limite per l’inertizzazione del medesimo, con polveri di CaCO3, non inferiore al 65% (Eckhoff, 2003), dato perfettamente allineato ai risultati sperimentali presentati. Infine, a proposito della capacità inertizzante dell’umidità presente nella polvere, si rileva come questa palesi capacità di aumento della MIE progressivamente crescenti all’aumentare del contenuto in peso. A questo proposito, la ex Guida CEI 31-56:2012 specifica quanto segue: “con percentuali di umidità superiori al 30%-50% la maggior parte delle polveri è inerte”. Si veda, al riguardo, il §5.3.2 del presente manuale.
Figura 2.18 – LFL/MEC & Pmax & Kst vs. dm [Polveri di zucchero]
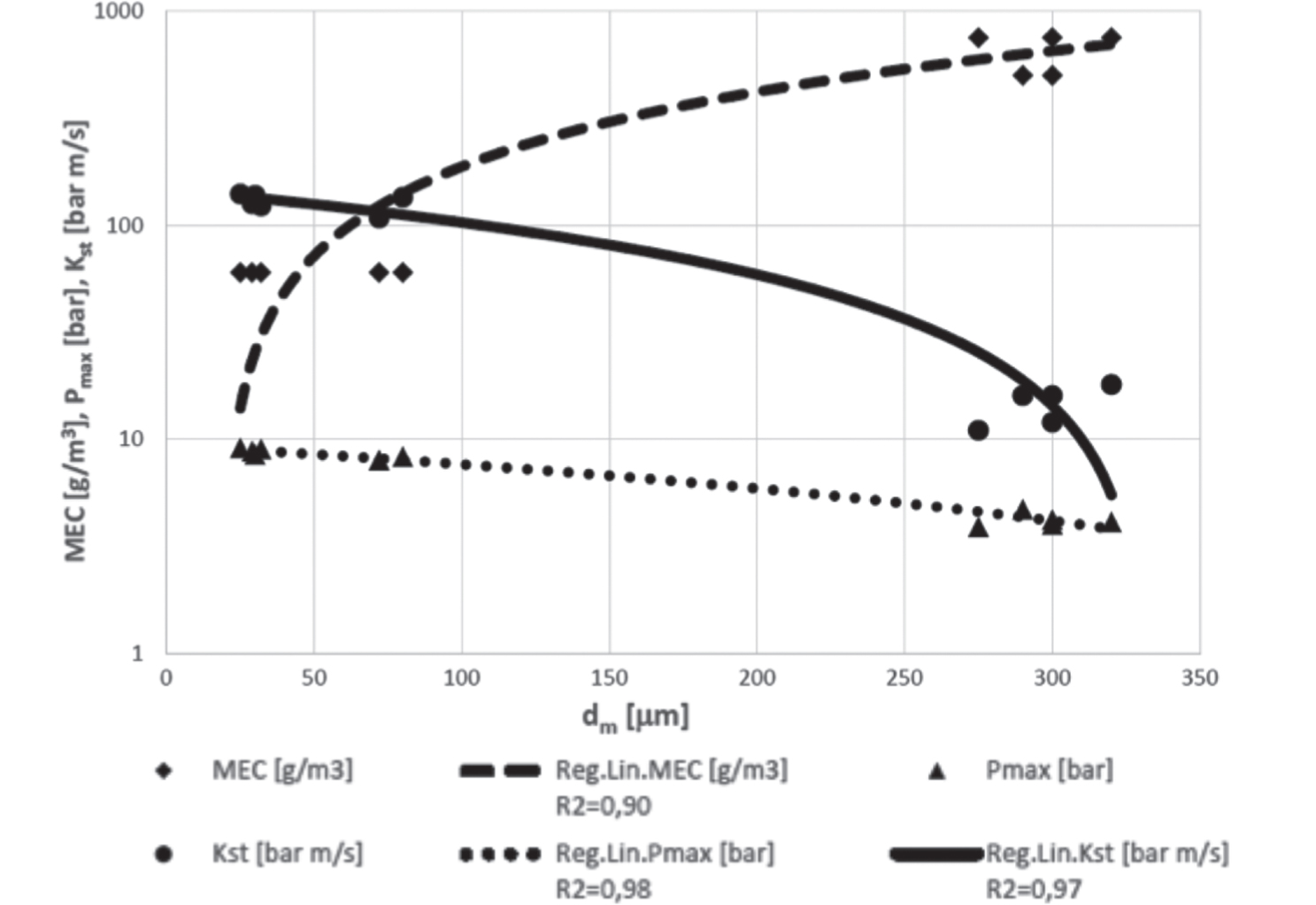
Fonte: BIA Report 13/1997
In ogni caso si vuole richiamare l’attenzione a non confondere l’umidità presente nella polvere con l’umidità atmosferica: sono parametri tra loro scollegati soprattutto in presenza di specifici processi di inumidimento e/o essicazione delle polveri. In ogni caso, relativamente all’umidità atmosferica, si può sintetizzare quanto riportato nel rapporto tecnico CLC/TR 60079-32-1 nei seguenti punti:
-
la resistività superficiale di alcuni materiali solidi isolanti può essere ridotta a livelli dissipativi se l’umidità relativa dell’aria viene mantenuta al di sopra del 65% (circa);
-
la superficie di alcuni materiali (es. vetro, fibre naturali) può adsorbire (…) umidità sufficiente a garantire la dissipatività (…);
-
non tutti i materiali, tuttavia, presentano la caratteristica appena esposta: non adsorbono umidità il PTFE, il PE, ecc.;
-
al di sotto del 30% (circa), i materiali sensibili all’umidificazione tornano (…) ad essere altamente isolanti.
A questo si aggiunga che d’inverno si verificano con maggiore frequenza esplosioni di polvere combustibile stante la grande disidratazione atmosferica. Una recente pubblicazione svedese (Huang, De Grahl, Nessvi, Lönnermark, Persson, 2019)30 afferma che [traduzione non ufficiale]: “La stagione secca invernale favorisce le esplosioni di polvere poiché le polveri hanno un basso contenuto di umidità e si disperdono più facilmente.
Figura 2.19 – MIE vs. Inerti & Umidità [Polveri di toner]
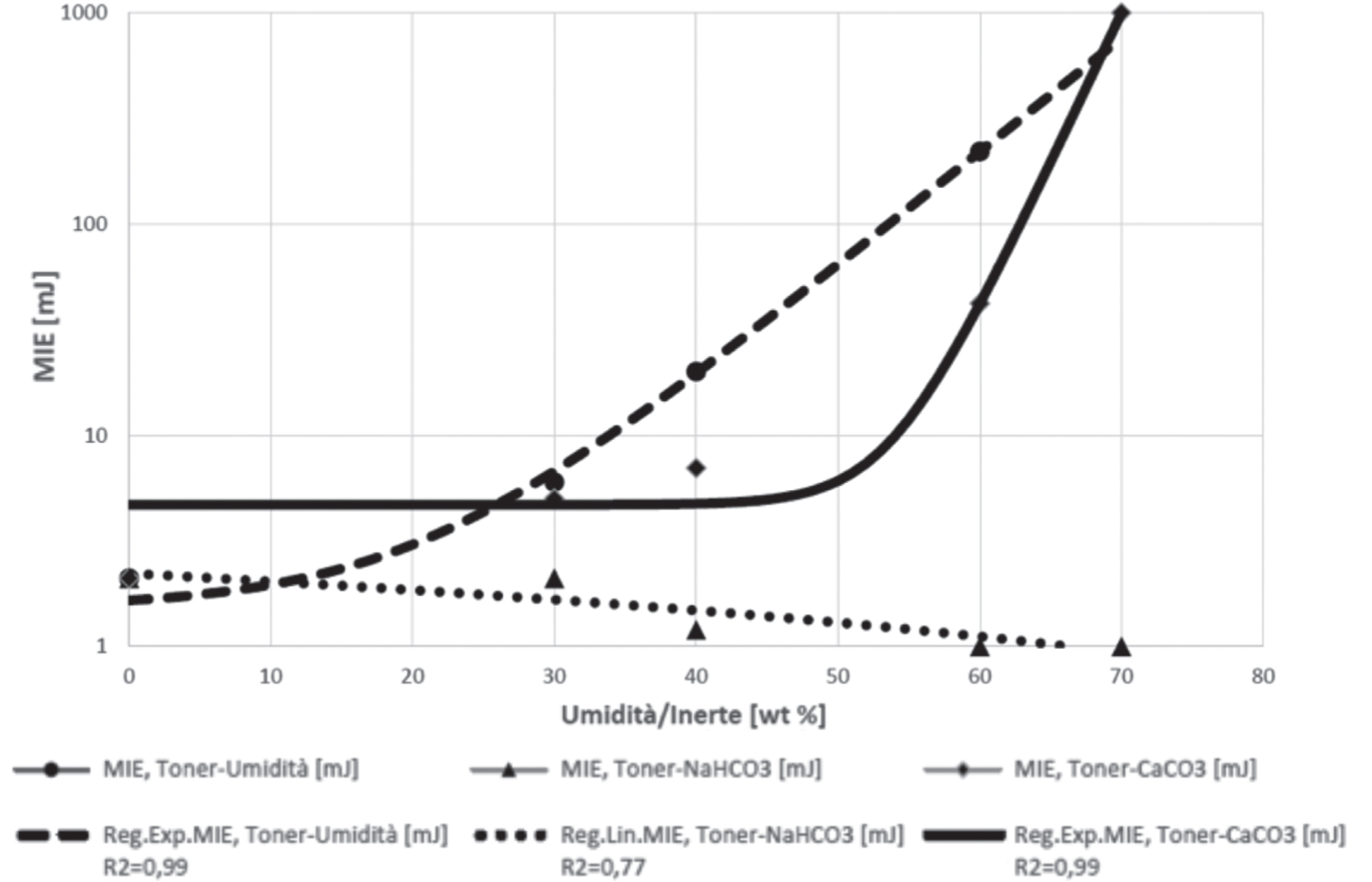
Fonte: Amez et al., 202331
L’analisi statistica dell’U.S. Chemical Safety Board (CSB, 2006)32 mostra che sette delle otto [grandi] esplosioni di polveri combustibili [avvenute in USA] tra il 1995 e il 2009 si sono verificate durante la stagione invernale (…)”.
Con modalità analoghe alle polveri di toner si comportano le polveri di licopodio, come appare evidente dalla Figura 2.20. Una crescita continua della MIE all’aumentare dell’umidità percentuale in massa.
La crescita percentuale dell’umidità in massa tende (cfr. Figura 2.21) ad avere i medesimi effetti dell’aumento della granulometria: aumenta l’LFL/MEC e diminuiscono i parametri di severità dell’esplosione.
La sintesi complessiva dei risultati è quindi sintetizzabile in Tabella 2.18, parametrizzando i seguenti parametri:
-
Kst (caratteristica specifica di esplodibilità)
-
Pmax (massima pressione di esplosione)
-
(dP/dt)max (massima velocità di incremento di pressione)
-
LFL/MEC (minima concentrazione esplosiva)
-
MIE (minima energia di accensione)
-
AIT (temperatura di accensione in nube)
al diametro medio delle polveri (dm) e/o umidità contenuta nelle polveri (Um).
Figura 2.20 – MIE vs. Umidità [Polveri di licopodio e toner]
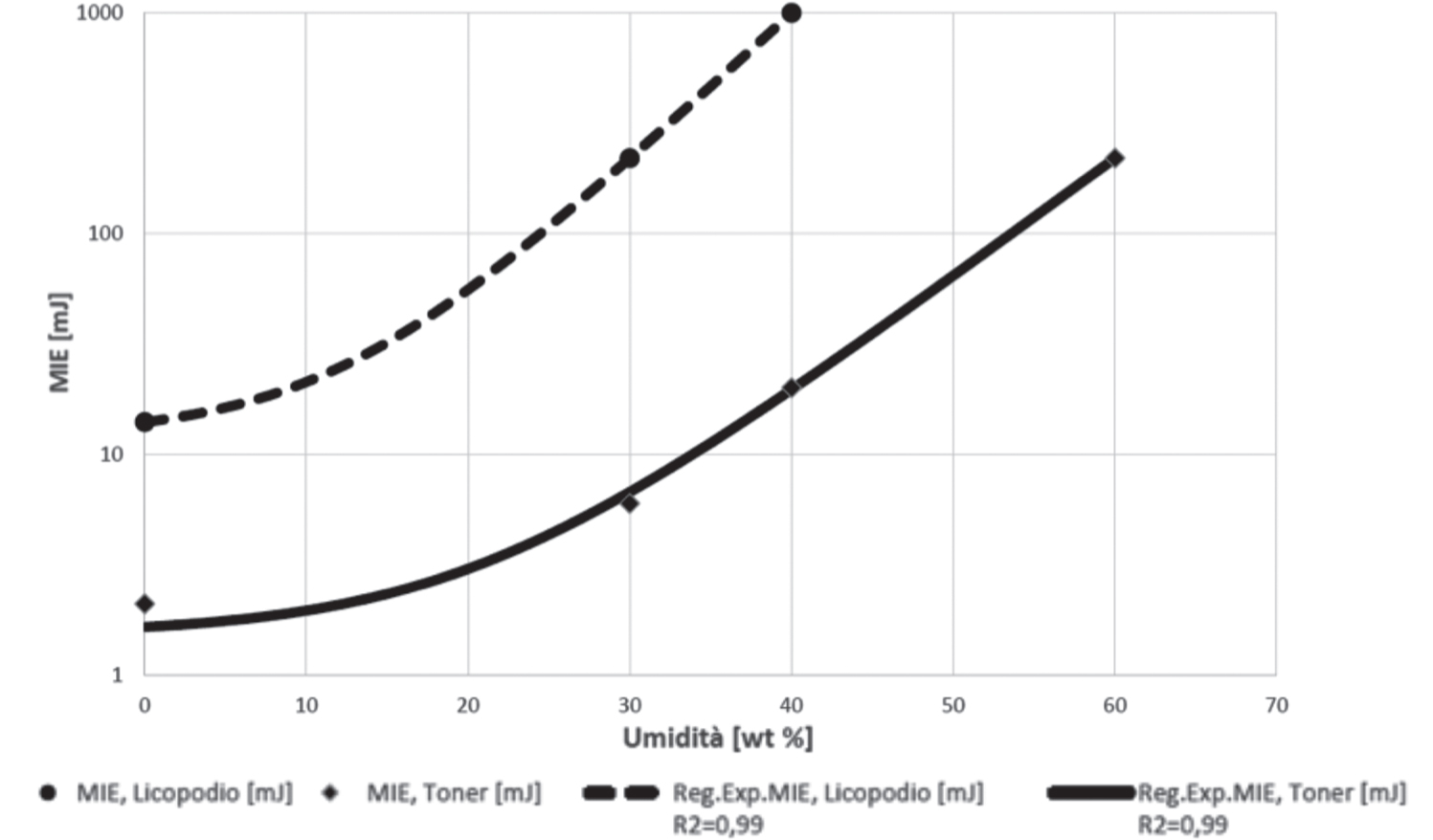
Fonte: Amez et al., 2023
Figura 2.21 – LFL/MEC & (dP/dt)max & Pex vs. Umidità [Polveri di carbone]
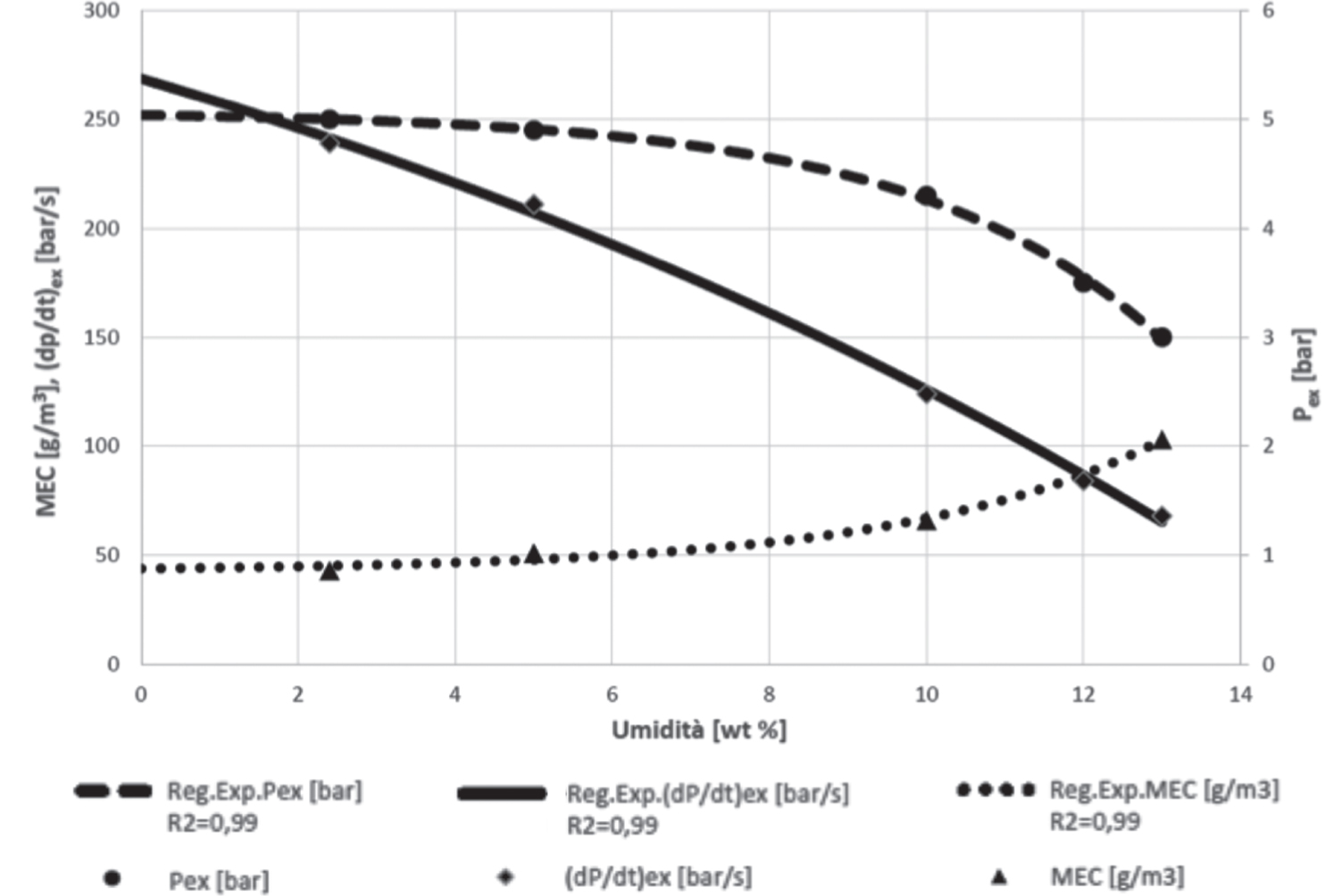
Tabella 2.18 – Sintesi della relazione tra i parametri di esplodibilità
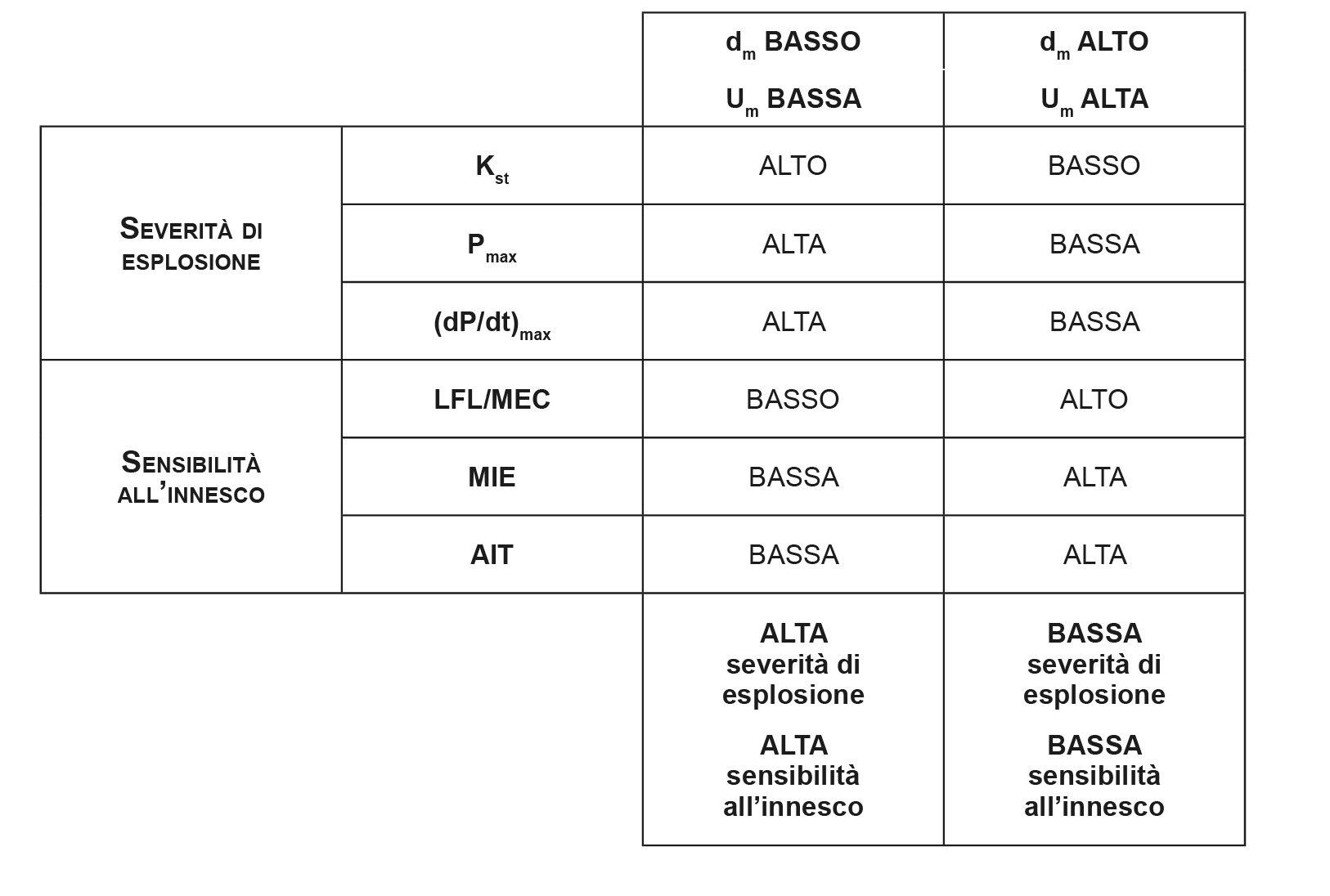
2.5 Parametri caratteristici di alcune sostanze
Si riportano in Tabella 2.19 e Tabella 2.20 i prospetti riepilogativi dei principali parametri di sicurezza di gas, vapori infiammabili e polveri combustibili presenti comunemente in ambito industriale. Essi sono tratti esclusivamente dalla migliore letteratura tecnica internazionale i cui riferimenti sono riportati a piè Tabella.
Risulta evidente che i parametri registrati sono relativi alla sostanza pura; qualsiasi operazione di interpolazione tra i dati qui presentati non è consigliabile se non supportata dagli strumenti di calcolo teorico propri della chimica industriale e/o da regole di calcolo presentate nella Normativa tecnica.
Appare inutile ricordare che i valori presentati sono indicativi; qualsiasi valutazione del rischio realizzata nell’ambito del Titolo XI, D.Lgs. n. 81/2008 dovrà essere esclusivamente supportata dalle schede di sicurezza del produttore delle sostanze/preparati presenti nel ciclo di produzione oppure ottenuti con la realizzazione di opportuni test di verifica effettuati in conformità alla Normativa indicata nei precedenti paragrafi.
Tabella 2.19 – Parametri di sicurezza delle principali sostanze (gas e vapori infiammabili) presenti in ambito industriale
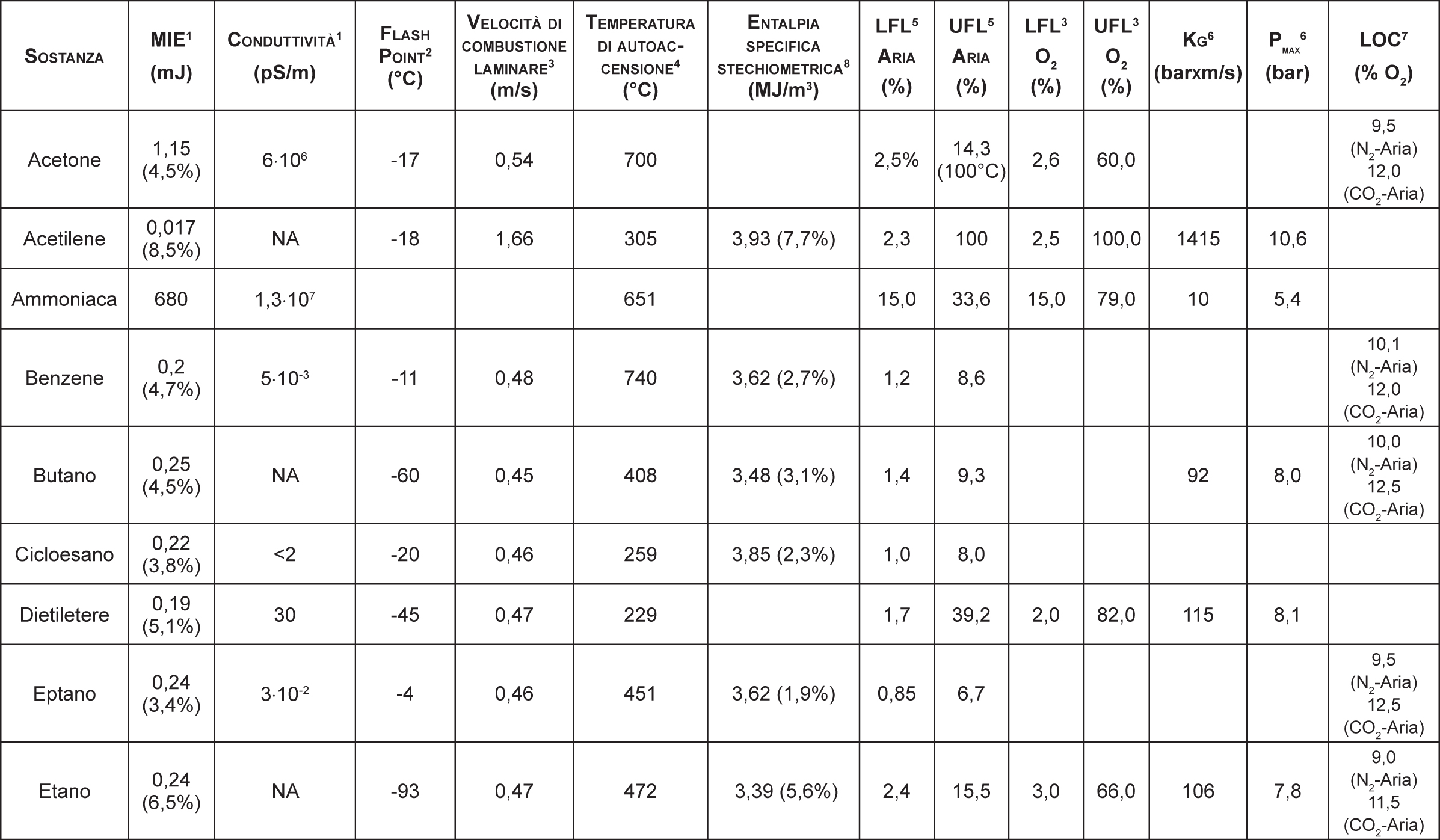
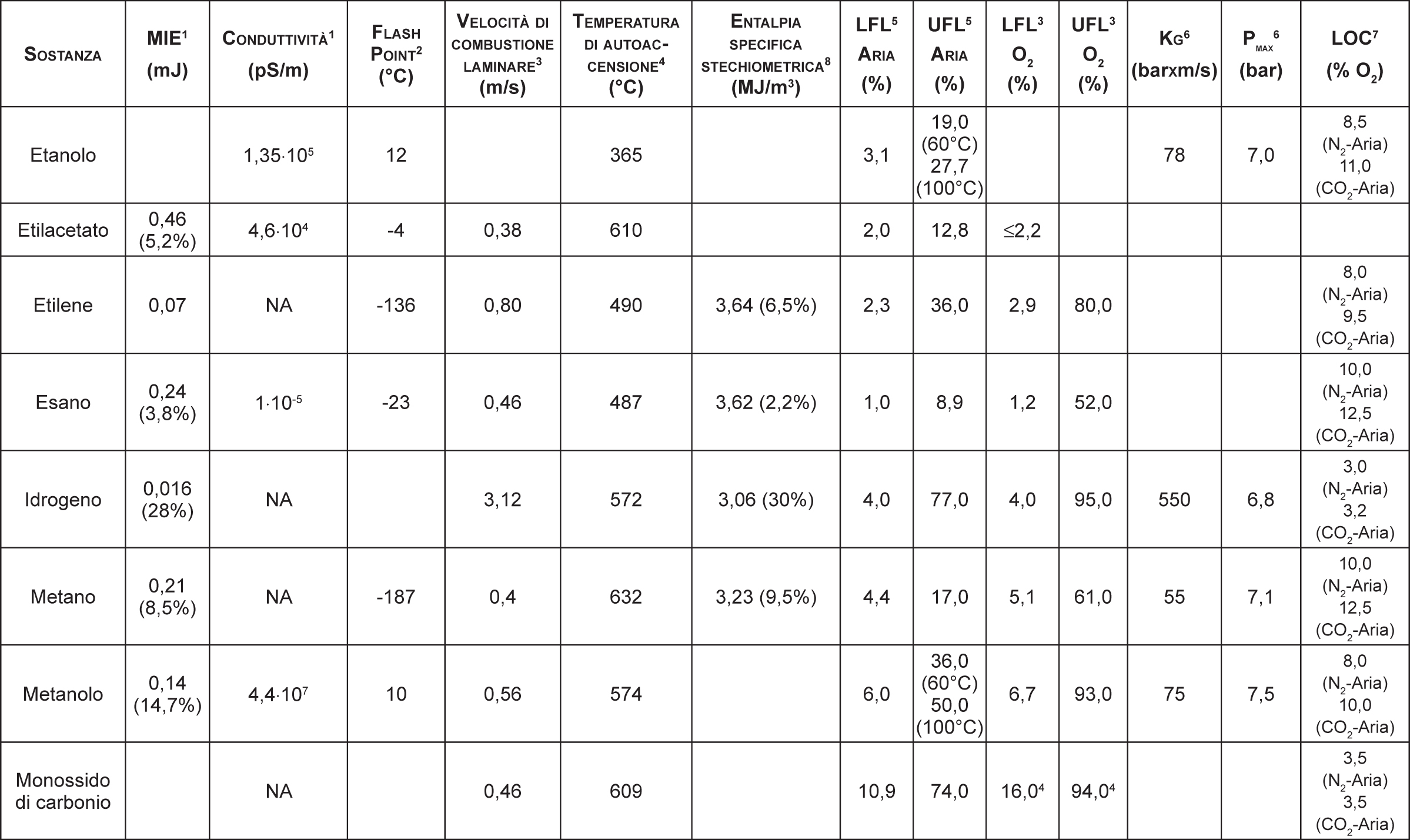
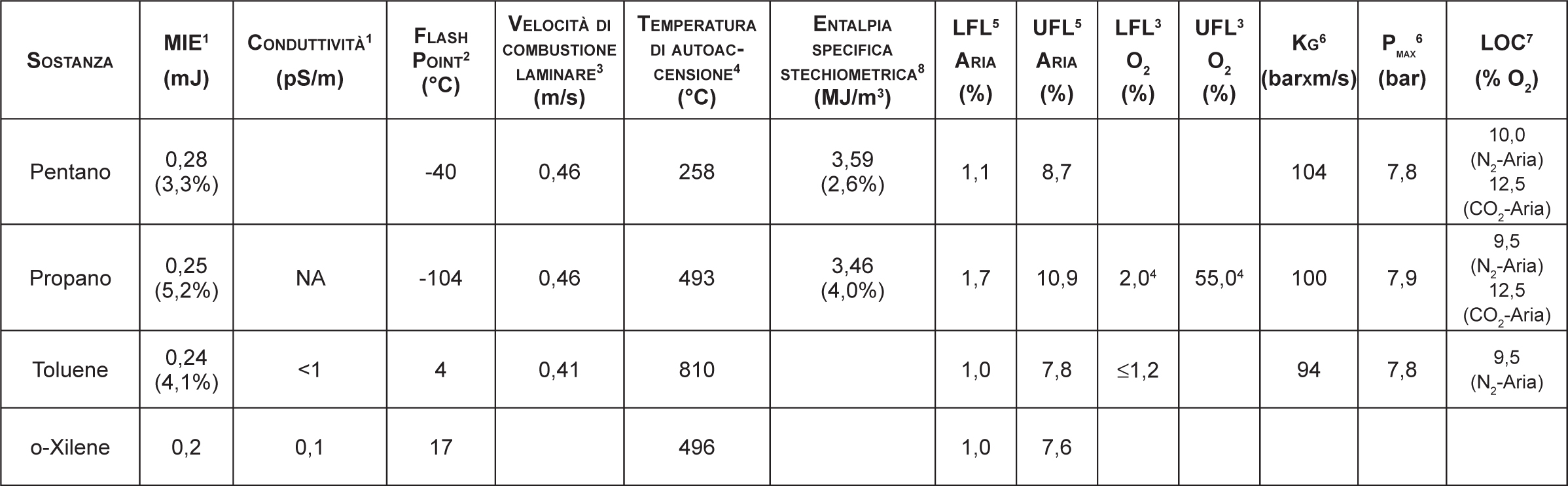
1 NFPA 77
2 Bretherick’s Handbook, 1999
3 NFPA Handbook, 2001
4 Glassman, 2008
5 IEC 60079-20-1
6 NFPA 68
7 NFPA 69
8 Harris, 1983
Tabella 2.20 – Parametri di sicurezza delle principali polveri combustibili presenti in ambito industriale
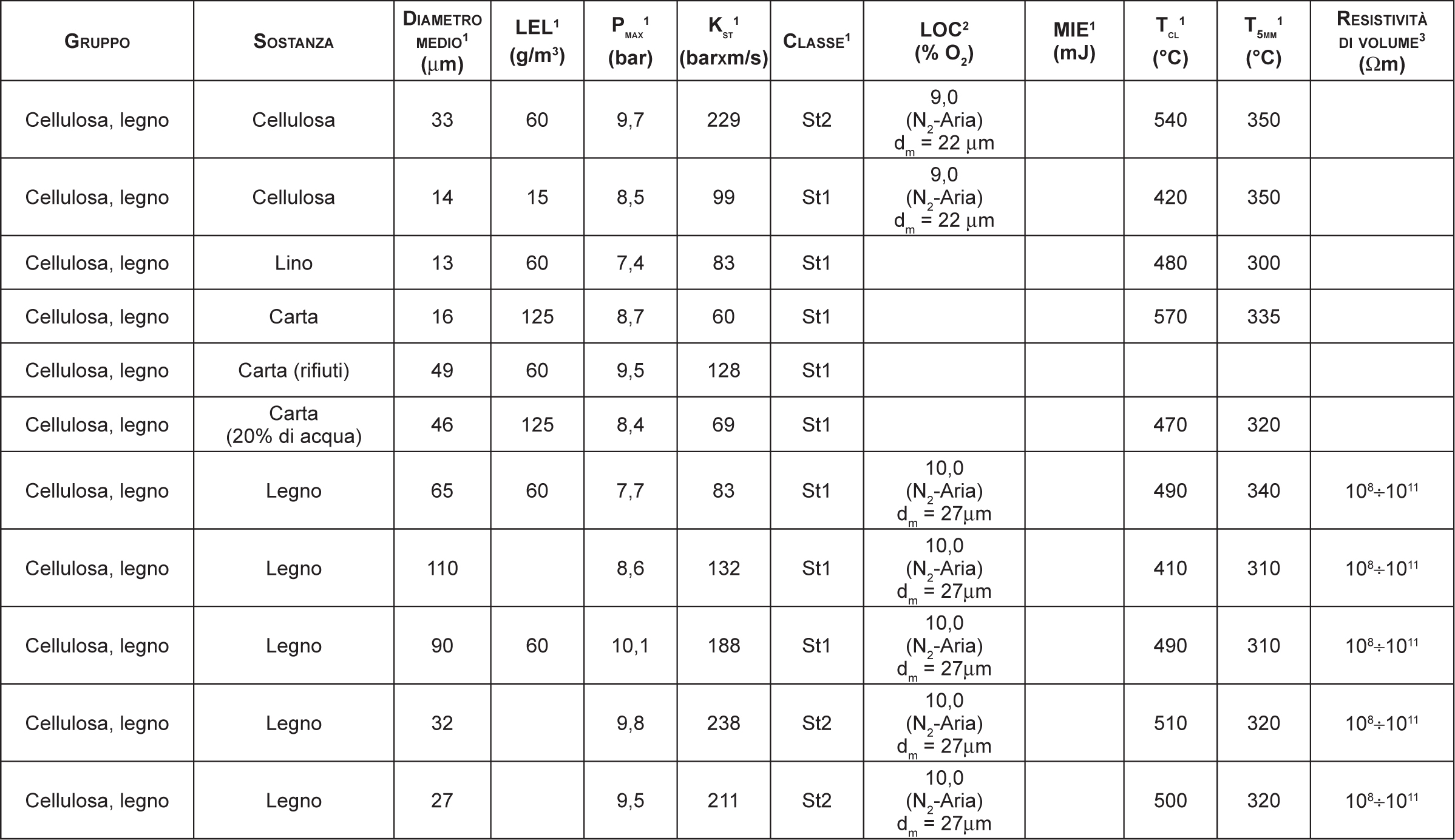
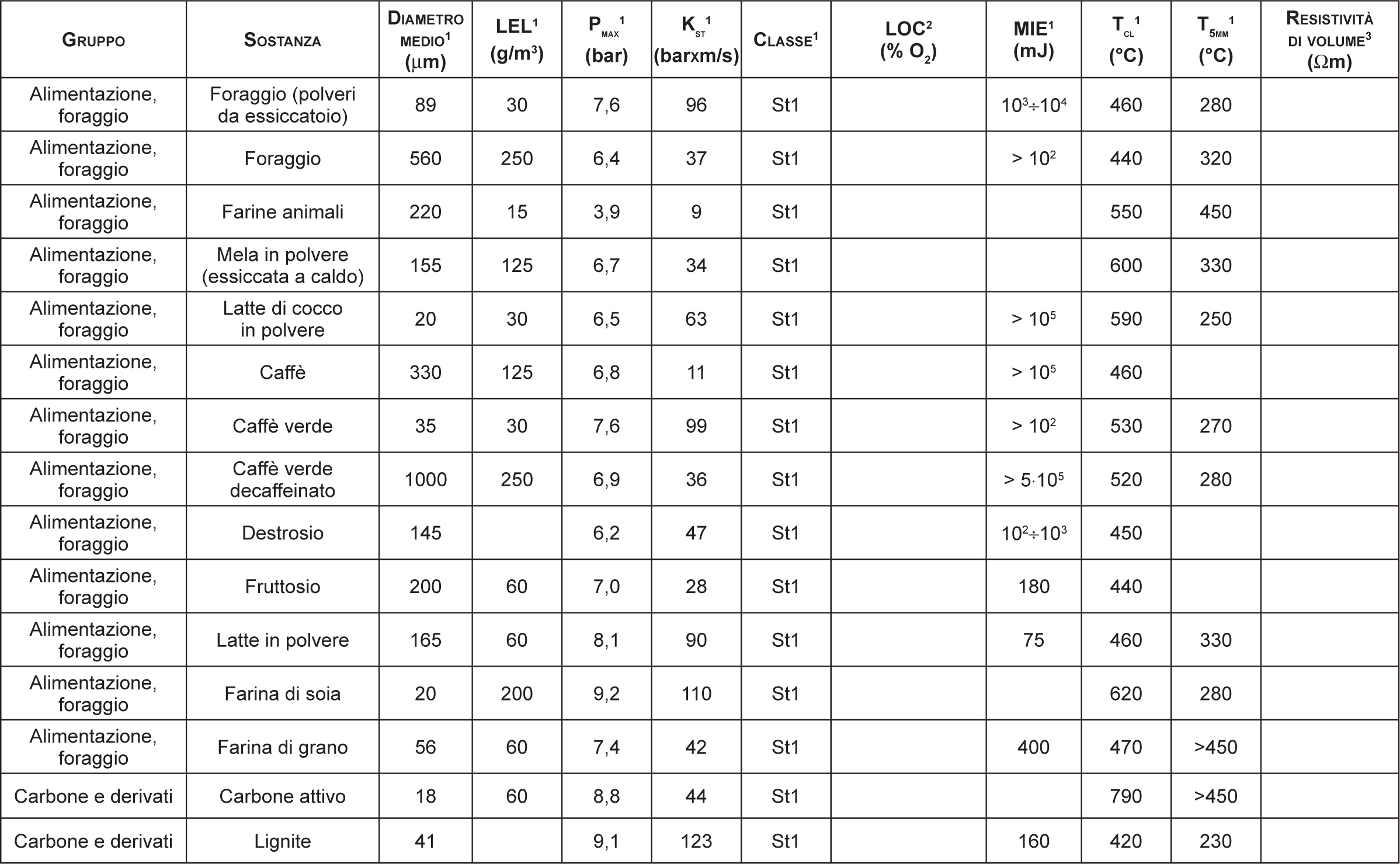
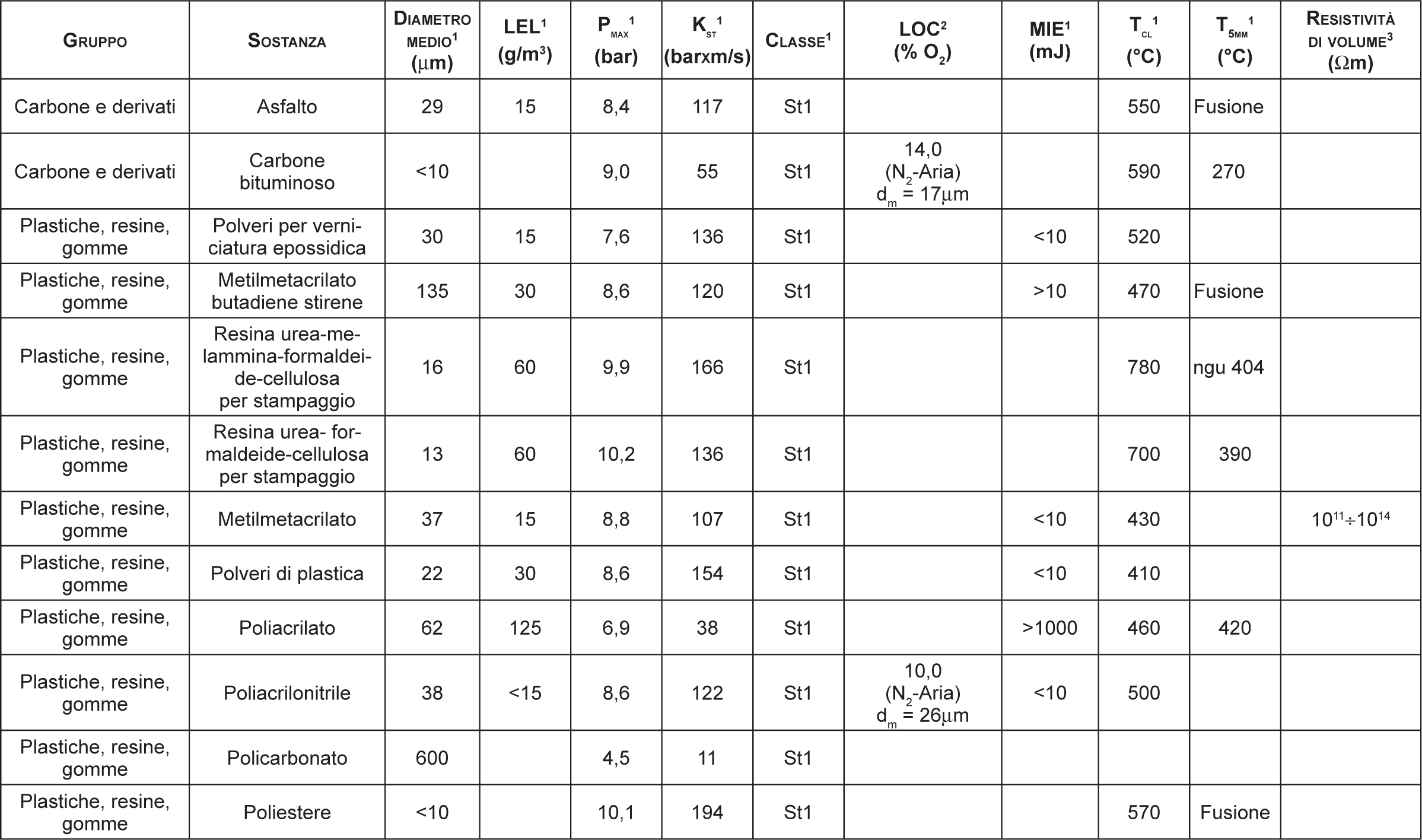
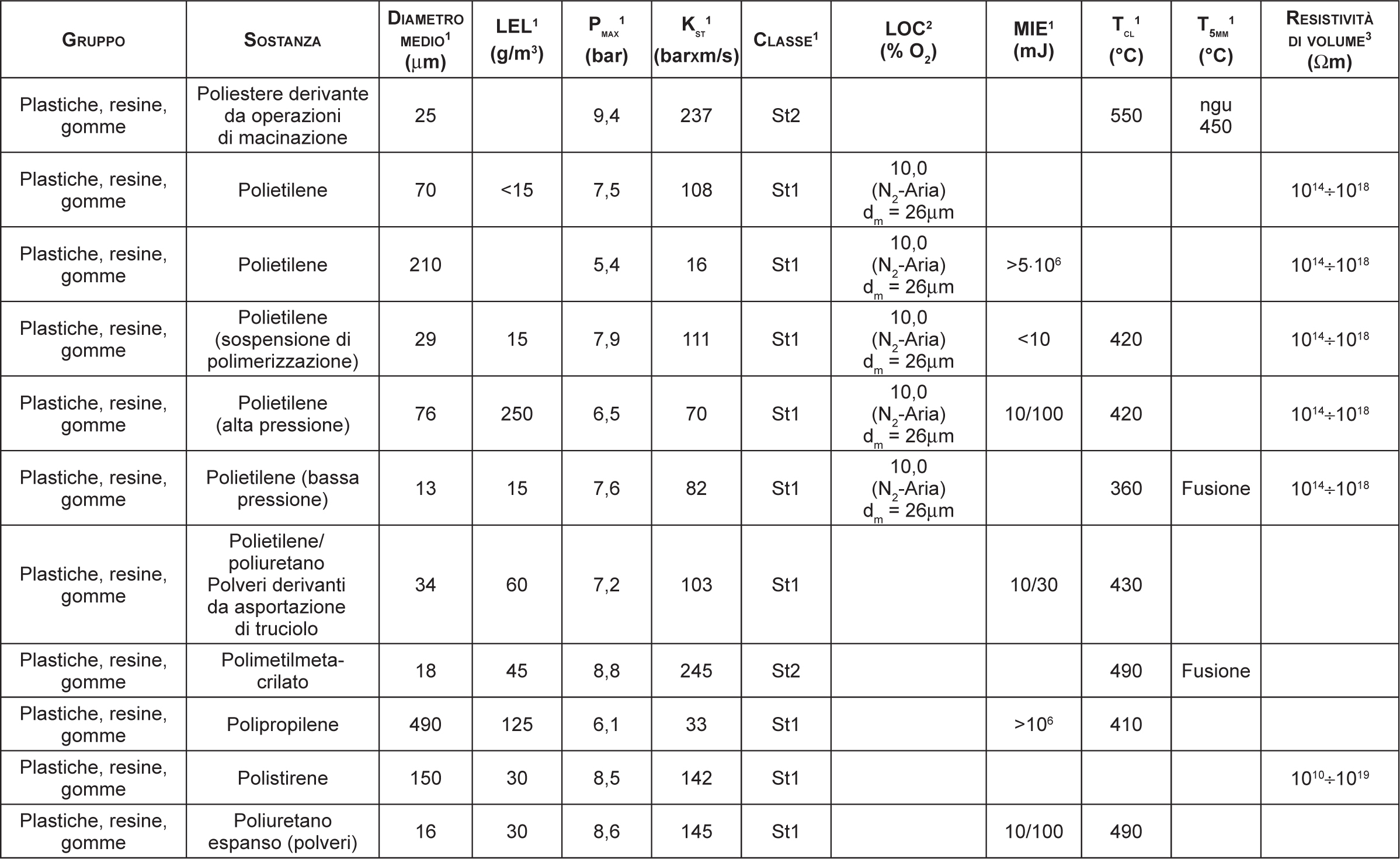
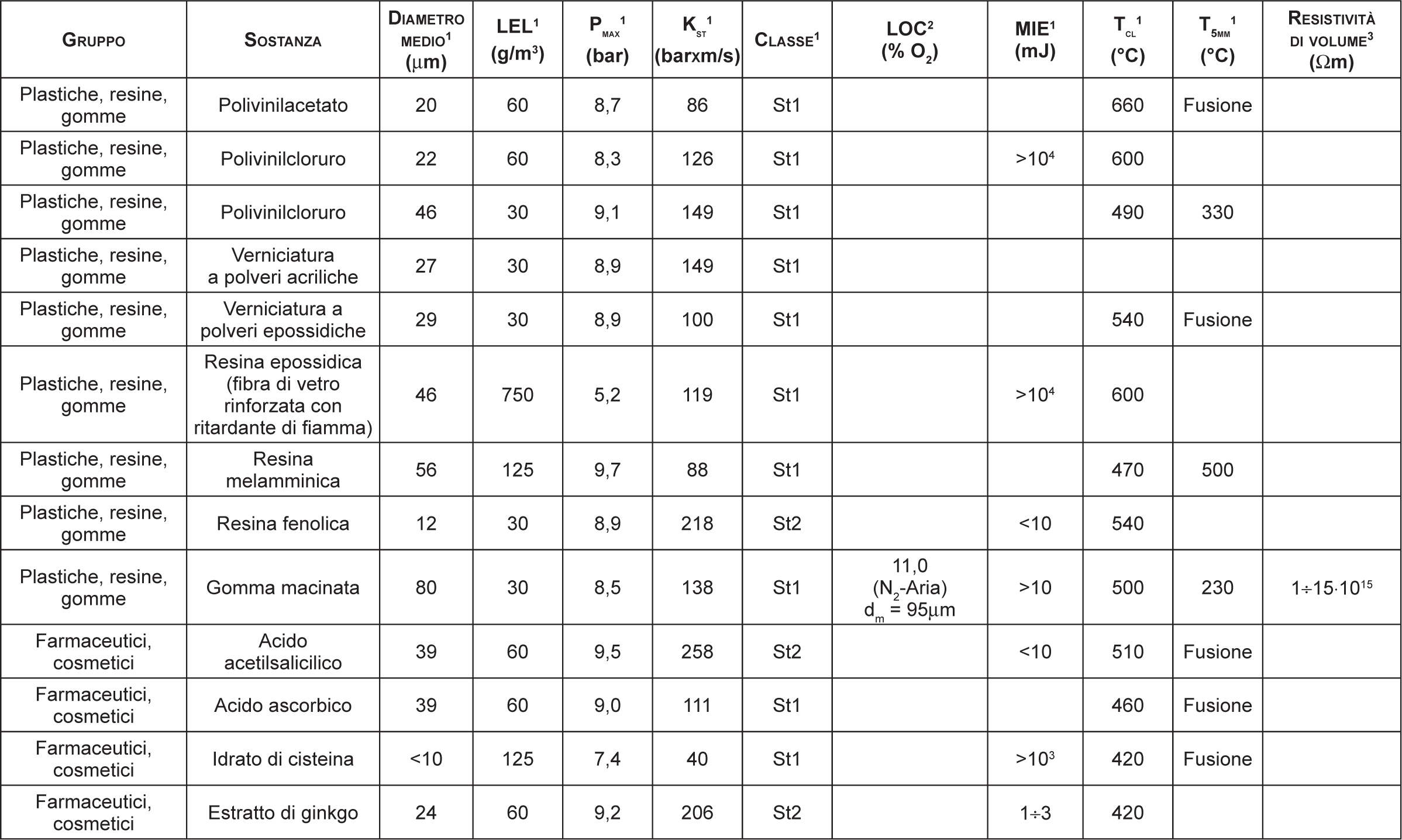
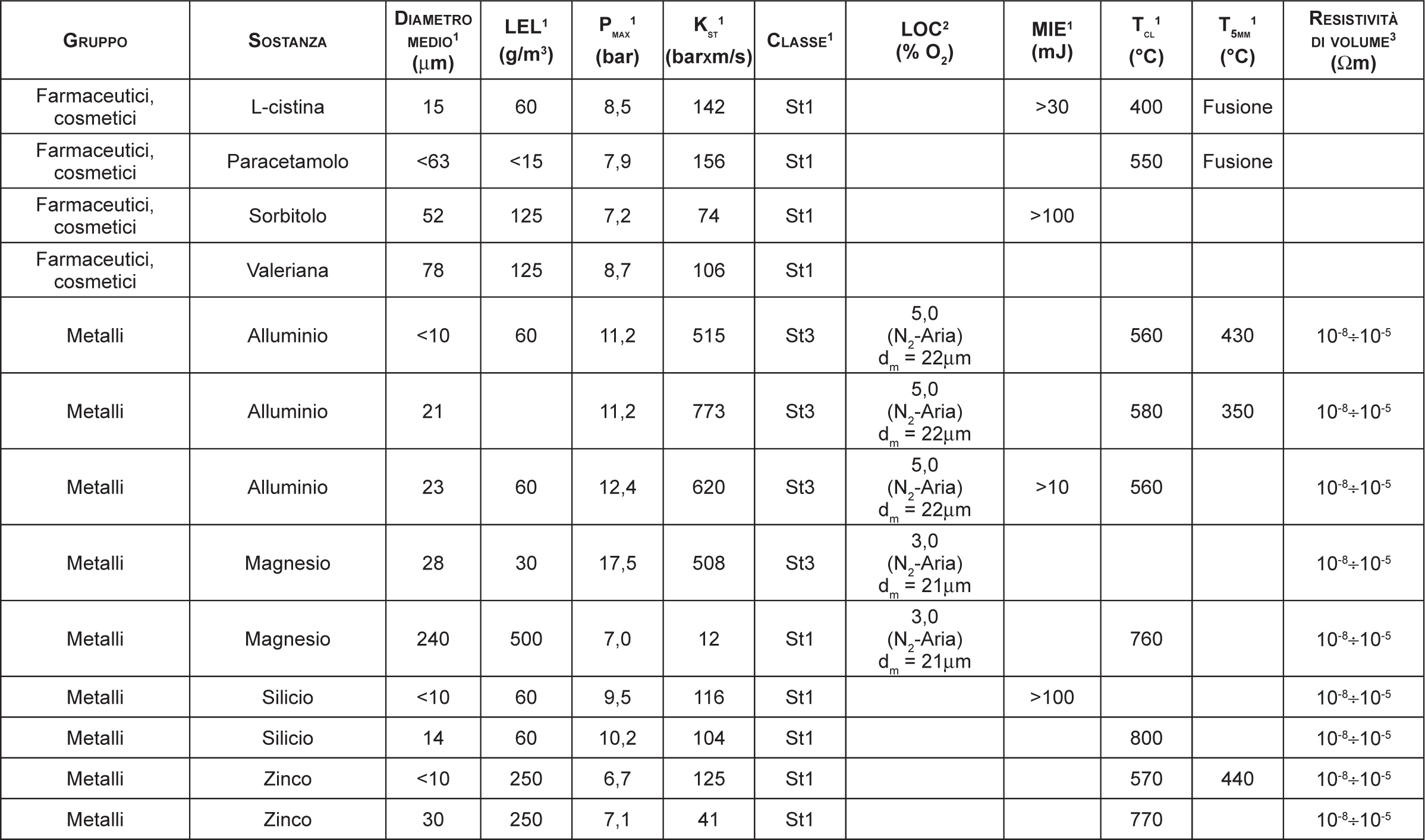
1 BIA, 1997 2 NFPA, 69 3 Pratt, 2000, ngu: nessuna emissione luminosa fino alla temperatura specificata